ДИМЕТИЛГИДРАЗИНЫ
C2H8N2, мол. м. 60,10; жидкости.
Несимметричный Д. (CH3)2NNH2;
т. пл. -57°С, т.кип. 62,8-63,8°С; d420 0,7911;
nD20 1,4084; h
0,51 мПа.с
(25 °С); DH0oбр-53,5
кДж/моль; очень гигроскопичен; смешивается с водой, этанолом и диэтиловым эфиром
во всех соотношениях. Сильное основание: рKa 7,21 (30 °С). Образует
устойчивые соли с к-тами, напр., кристаллич. гидрохлорид (т. пл. 81-82°С).
Подробнее о хим. св-вах см. Гидразина замещенные органические
.
В пром-сти его получают: 1) нитрозированием диметиламина
нитритами щелочных металлов в кислой среде с послед. восстановлением (кат.-
Pd или Pt) образовавшегося диметилнитрозамина:
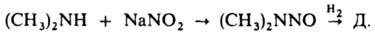
2) взаимод. диметиламина с монохлорамином:

3) восстановительно-каталитич. алкилированием ацетилгидразида формальдегидом и Н2 с послед. щелочным гидролизом образовавшегося диметилацетилгидразида (способ осуществлен в США):

несим-Д.- горючий компонент ракетного топлива (многотоннажный продукт).
Раздражает кожу, слизистые оболочки глаз и дыхат. путей; ПДК 1 мг/м3.
Симметричный Д. CH3NHNHCH3, т.кип. 81 °С; d420 0,8274; nD20 1,4209; т.пл. дигидрохлорида 165-167 °С. Обычно его синтезируют ацилированием гидразина с послед. метилированием полученного диацилгидразида диметилсульфатом и омылением образовавшегося диацилдиметилгидразида:
NH2NH2 + 2RCOCl : RCONHNHCOR : RCON(CH3)N(CH3)COR : CH3NHNHCH3
Лит.: Иоффе Б. В., Кузнецов М. А., Потехин А. А., Химия органических производных гидразина, Л., 1979; Большаков Г. Ф., Химия и технология компонентов жидкого ракетного топлива. Л., 1983; Kirk-Othmer encyclopedia, 3 ed., v. 12, N.Y., 1980, p. 739. С. А. Поддубная.
|

