ФТОРИСТОВОДОРОДНАЯ КИСЛОТА
(фтороводородная к-та), р-р фтористого водорода
в воде. Устар. назв.-
плавиковая к-та. В системе HF - H2O могут существовать 3 соед.: H2O·HF
(H3O+F-), H2O·2HF (H3O+HF2-)
и H2O·4HF, т.пл. к-рых соотв. -36, -78 (с разл.) и -100 0C;
т.пл. эвтектич. смеси H2O - H2O·HF -72 0C;
для азеотропной смеси (38,2% по массе HF) т. кип. 114,5 0C. При всех
составах, отличных от азеотропного, Ф. к. испаряется инконгруэнтно. Равновесное
давление паров HF и H2O над Ф.к. описывается ур-нием lgр(Пa)
= A — В/Т, значения коэф. см. в табл.
|
|
|
|
|
|
|
|
|
|
Концентрация HF,
% по массе
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Для р-ров HF + nH2O
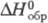 -317,74
кДж/моль (n = 1), -322,03
кДж/моль (n = 10), -322,36 кДж/моль (n = 100) и -335,65
кДж/моль (n =
-317,74
кДж/моль (n = 1), -322,03
кДж/моль (n = 10), -322,36 кДж/моль (n = 100) и -335,65
кДж/моль (n = 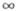 ).
Ф.к. содержит ионы H+, F-, HF2-,
H3O+, (HF)nF- и молекулы
H3O+(HF)nF- с n =
1 - 4. Плотность Ф.к. при 25 0C меняется от 1,00132 г/см3
(0,20 моль/дм3) до 1,07099 г/см3 (11,40 моль/дм3);
электрич. проводимость при -6
0C - от 1,90 мкСм/см (0,0472 моль/дм3) до 54,36 мкСм/см
(2,82 моль/дм3). Ф. к.- сильная к-та, рКа 3,14;
образует соли -фториды
; реагирует со мн. в-вами, в т. ч. с такими оксидами,
как SiO2, B2O3, Nb2O5,
Ta2O5, MoO3, WO3, и силикатами.
).
Ф.к. содержит ионы H+, F-, HF2-,
H3O+, (HF)nF- и молекулы
H3O+(HF)nF- с n =
1 - 4. Плотность Ф.к. при 25 0C меняется от 1,00132 г/см3
(0,20 моль/дм3) до 1,07099 г/см3 (11,40 моль/дм3);
электрич. проводимость при -6
0C - от 1,90 мкСм/см (0,0472 моль/дм3) до 54,36 мкСм/см
(2,82 моль/дм3). Ф. к.- сильная к-та, рКа 3,14;
образует соли -фториды
; реагирует со мн. в-вами, в т. ч. с такими оксидами,
как SiO2, B2O3, Nb2O5,
Ta2O5, MoO3, WO3, и силикатами.
Ф.к. получают р-рением
HF в воде, водной абсорбцией газообразных продуктов сернокислотного разложения
CaF2, пирогидролизом CaF2, UF6, фторидов др.
металлов, флюори-товых руд и фторсодержащих отходов произ-в. Ф. к.- реагент
в произ-ве AlF3, UF3 и др. неорг. фторидов, компонент
р-ров для травления стекол, кварца, материалов микроэлектроники, металлов и
нек-рых сплавов.
Ф. к. при попадании на
кожу вызывает болезненные ожоги, причем действие разб. Ф.к. проявляется через
неск. часов после поражения.
Хранят Ф. к. в гумир. или
полиэтиленовых емкостях.
Э.Г. Раков.



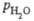
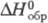 -317,74
кДж/моль (n = 1), -322,03
кДж/моль (n = 10), -322,36 кДж/моль (n = 100) и -335,65
кДж/моль (n =
-317,74
кДж/моль (n = 1), -322,03
кДж/моль (n = 10), -322,36 кДж/моль (n = 100) и -335,65
кДж/моль (n = 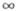 ).
Ф.к. содержит ионы H+, F-, HF2-,
H3O+, (HF)nF- и молекулы
H3O+(HF)nF- с n =
1 - 4. Плотность Ф.к. при 25 0C меняется от 1,00132 г/см3
(0,20 моль/дм3) до 1,07099 г/см3 (11,40 моль/дм3);
электрич. проводимость при -6
0C - от 1,90 мкСм/см (0,0472 моль/дм3) до 54,36 мкСм/см
(2,82 моль/дм3). Ф. к.- сильная к-та, рКа 3,14;
образует соли -
).
Ф.к. содержит ионы H+, F-, HF2-,
H3O+, (HF)nF- и молекулы
H3O+(HF)nF- с n =
1 - 4. Плотность Ф.к. при 25 0C меняется от 1,00132 г/см3
(0,20 моль/дм3) до 1,07099 г/см3 (11,40 моль/дм3);
электрич. проводимость при -6
0C - от 1,90 мкСм/см (0,0472 моль/дм3) до 54,36 мкСм/см
(2,82 моль/дм3). Ф. к.- сильная к-та, рКа 3,14;
образует соли -