ГЕСТАГЕНЫ
(от лат. gesto-ношу и греч. -genes-рождающий, рожденный)
(прогестины, гормоны желтого тела), гормоны регулирующие беременность у
плацентарных животных. Относятся к С21-стероидам, в основе к-рых
лежит скелет прегнана (ф-ла I).
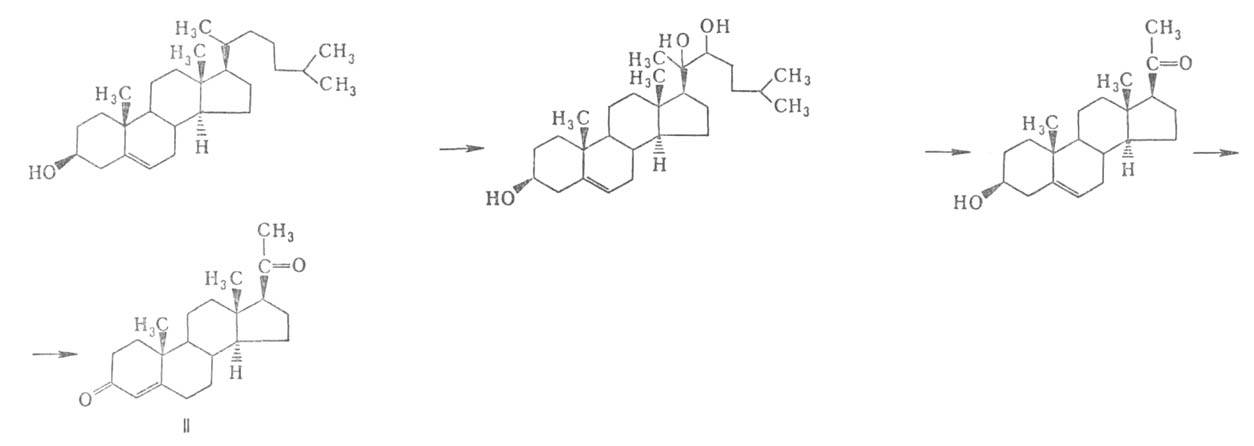
Важнейший прир. Г.-4-прегнен-3,20-дион, или прогестерон (II; т. пл.
128-130 °С). Его биосинтез осуществляется из холестерина, гл. обр. в надпочечниках,
плаценте и желтом теле (см. ур-ние р-ции).
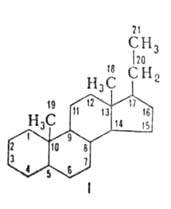
Превращ. 20,22-дигидроксихолестерина в 3 гидрокси-5-прегнен-20-он
происходит с участием кофермента никотинамидадениндинуклеотид-фосфата (НАДФ),
дегидрирование гидроксильной группы в положении 3, сопровождающееся миграцией
двойной связи из положения 5 в положение 4, осуществляется с участием фермента
дегидрогеназы и кофермента никотинамидадениндинуклеотида (НАД). Прогестерон,
синтезируемый в надпочечниках, по-видимому, не поступает в кровь и используется
наряду с прегненолоном (его предшественником в биосинтезе) для биосинтеза
кортикоидов. Гормональные ф-ции выполняет прогестерон, синтезируемый в
яичниках и семенниках, что позволяет рассматривать Г. как гормоны местного
действия. Биол. роль Г. у плацентарных животных состоит в подготовке слизистой
матки к имплантации зародыша и сохранении его во время беременности (гестагенное
действие). Наряду с эстрогенами и пептидными гормонами (лютеинизирующим
и фоликулостимулирующим) Г. участвуют в регуляции женского полового цикла,
причем все эти гормоны взаимно регулируют свой биосинтез. Прогестерон взаимодействует
с рецепторами клеток матки, влияет на проницаемость клеточной мембраны
для электролитов и пр. Метаболизм Г. происходит гл. обр. в печени, где
восстанавливаются карбонильные группы и двойная связь, в яичниках, где
осуществляется биосинтез из Г. эстрогенов, и в надпочечниках.
гидрокси-5-прегнен-20-он
происходит с участием кофермента никотинамидадениндинуклеотид-фосфата (НАДФ),
дегидрирование гидроксильной группы в положении 3, сопровождающееся миграцией
двойной связи из положения 5 в положение 4, осуществляется с участием фермента
дегидрогеназы и кофермента никотинамидадениндинуклеотида (НАД). Прогестерон,
синтезируемый в надпочечниках, по-видимому, не поступает в кровь и используется
наряду с прегненолоном (его предшественником в биосинтезе) для биосинтеза
кортикоидов. Гормональные ф-ции выполняет прогестерон, синтезируемый в
яичниках и семенниках, что позволяет рассматривать Г. как гормоны местного
действия. Биол. роль Г. у плацентарных животных состоит в подготовке слизистой
матки к имплантации зародыша и сохранении его во время беременности (гестагенное
действие). Наряду с эстрогенами и пептидными гормонами (лютеинизирующим
и фоликулостимулирующим) Г. участвуют в регуляции женского полового цикла,
причем все эти гормоны взаимно регулируют свой биосинтез. Прогестерон взаимодействует
с рецепторами клеток матки, влияет на проницаемость клеточной мембраны
для электролитов и пр. Метаболизм Г. происходит гл. обр. в печени, где
восстанавливаются карбонильные группы и двойная связь, в яичниках, где
осуществляется биосинтез из Г. эстрогенов, и в надпочечниках.
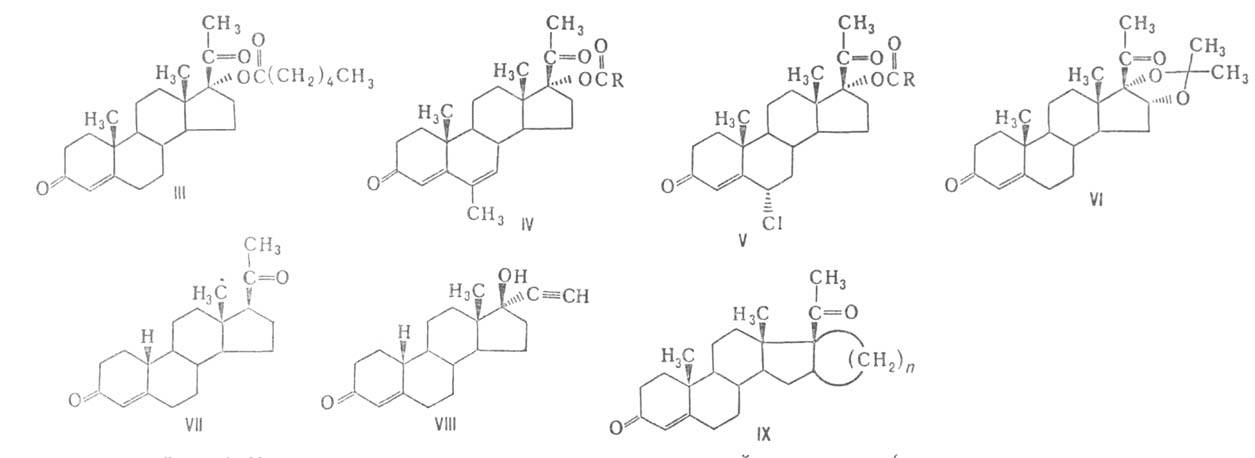
Среди синтетич. стероидов найдены в-ва, превосходящие по своей активности
природные и, в отличие от прогестерона, активные при оральном введении.
наиб. известны соед. следующих четырех типов: производные прогестерона,
содержащие заместители в положениях 6,16,17 [напр., делалутин (III), мегестролацетат
(IV, R = СН3), хлормадинонацетат (V; R = СН3), олгестон
ацетонид (VI) и его аналоги с атомом N или S вместо кислородного], производные
19-норпрогестерона (VII), эстрана [напр., норэтиндрон (VIII)] и прегна-В-пентараны
(IX; и = = 1-5). У большинства 20-кетопрегнанов вращение ацетильной группы
в положении 17 заторможено и преимущественная конформация имеет торсионный
угол С(16)-С(17)--С(20)-О(20) от 10 до 40°.
Нек-рые модифицированные Г. обнаруживают наряду с гестагенной активностью
(или вместо нее) зстрогенное, андрогенное или антиандрогенное действие.
К последним относится, напр., ципротерон (см. ф-лу IV в ст. Андрогены
).
Хим. модификация Г. направлена гл. обр. на поиск оральных противозачаточных
ср-в и Г. с оптимальной физиол. активностью.
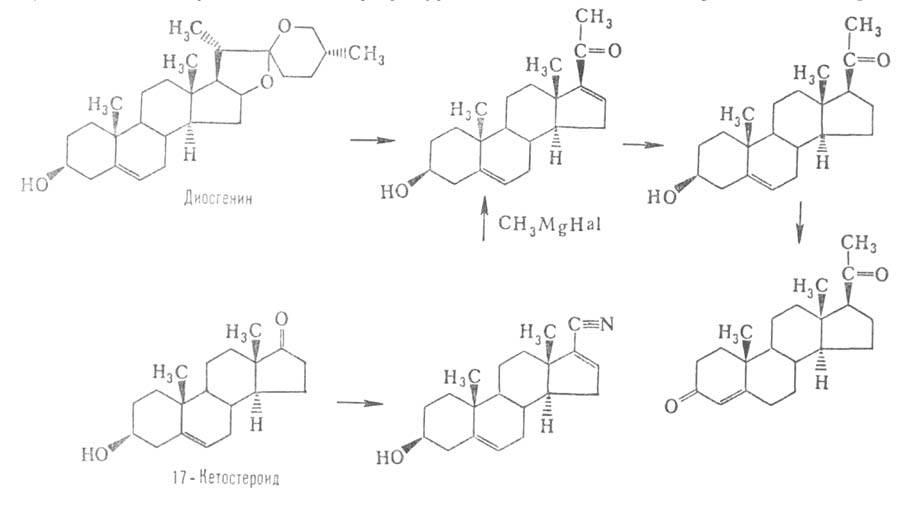
Пром. синтез прогестерона осуществляется из диосгенина (вместо него
используют также соласодин) или из 17-кетостероидов (см. ур-ние р-ции).
Г. применяют при нарушениях овариально-менструального цикла, аменорее,
функциональных кровотечениях, для предупреждения выкидышей, а также в качестве
противозачаточных ср-в (обычно в комбинации с эстрогенами).
Лит.: Савченко О.Н., Степанова Н.А., в кн.: Физиология эндокринной
системы, Л., 1979, с. 396-413; Ре trow V., Steroidal oral contraceptive
agents, в кн.: Essays in biochemistry, ed. by P. N. Campbell, G.D. Greville,
v. 2, L.-N.Y., 1966, p. 117-45; Kamernitzky A. V., "Heterocycles", 1977,№
7(1), p. 547-91; Kaonernitzky A.V. [a.o.], "Journal of Steroidic Biochemistry",
1982, v. 16, № I, p. 61-67. См. также лит
. при ст. Стероиды
. А. В. Камерницкий.

