ГРИНЬЯРА РЕАКЦИЯ
, синтез орг. соединений с применением магнийорг.
галогенидов RMgHal (реактивов Гриньяра). Последние обычно получают по р-ции:
RHal + Mg -> RMgHal. При этом р-р RHal в диэтиловом эфире медленно при
перемешивании прибавляют к суспензии Mg в этом же р-рителе. Во мн. случаях
(особенно при работе с ArHal) магний активируют, для чего в реакц. смесь
добавляют I2, BrCH2CH2Br или С2Н5Вг.
Для синтеза RMgHal из СН2=СННа1 и ArCl вместо диэтилового эфира
применяют ТГФ или др. циклич. эфиры, а также эфиры ди-и триэтиленгликоля.
Из соед., содержащих подвижный атом Н (ацетилены, пиррол, индол и др.),
реактив Гриньяра получают обменной р-цией, напр.:
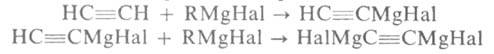
Активность RHal уменьшается в ряду: RI > RBr > RC1.
При получении реактива Гриньяра на практике применяют RBr, т.к. RC1
мало реакционноспособен, а р-ции с RI сопровождаются побочными процессами
в большей степени, чем с бромидами. В случае вторичных и особенно третичных
RI наблюдается отщепление HI с образованием олефина. Другая побочная р-ция,
к-рая часто сопровождает синтез алкилмагнийгалогенидов,-образование углеводородов
(р-ция Вюрца-Гриньяра): RHal + RMgHal -> R—R + MgHal2. В присут.
каталитич. кол-в солей переходных металлов образуется обычно R—R (р-ция
Хараша).
Магнийорг. галогениды чрезвычайно реакционноспо-собны. наиб. широко
их применяют в р-циях с соед., содержащими поляризованную кратную связь
(напр., С=O, С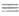 N,
C=S).
N,
C=S).
При взаимод. RMgHal с формальдегидом, оксидом этилена или этиленхлоргидрином
образуются первичные спирты, из др. альдегидов и формиатов (эфиров)- вторичные,
из кетонов, ангидридов, хлорангидридов и сложных эфиров-третичные, напр.:
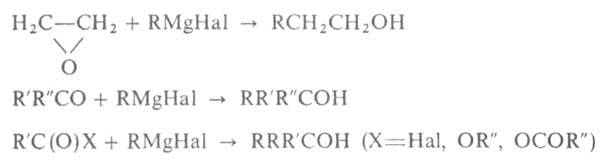
Р-цию RMgHal с ангидридами и хлорангидридами в спец. условиях используют
для синтеза кетонов, напр.:
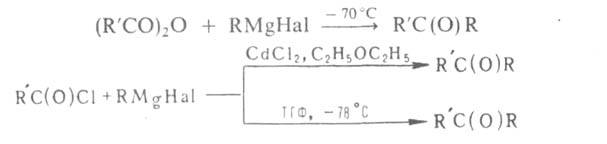
Наиб. широко для синтеза кетонов применяют амиды к-т и нитрилы:
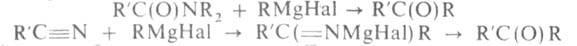
Кетоны образуются также в Г. р. с применением орто-угольных эфиров:
C(OR)4 + RMgHal -> RRC(OR)2 -> RC(O)R Удобный метод
синтеза альдегидов-р-ции с использованием ортомуравьиного эфира; вместо
него применяют также формиаты (эфиры и соли) и формамиды (обычно N-метилформанилид):
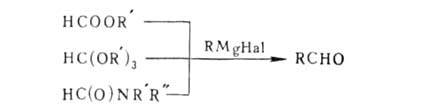
Взаимод. RMgHal с СО2 синтезируют карбоновые к-ты, с диалкилкарбонатами
и ортоугольным эфиром-эфиры и ортоэфиры карбоновых к-т.
Во мн. случаях Г. р. с карбонильными соед. протекают с количеств. выходом.
Затруднения возникают при синтезе в-в с разветвленными радикалами. наиб.
распространенные побочные р-ции-енолизация и восстановление, напр.:
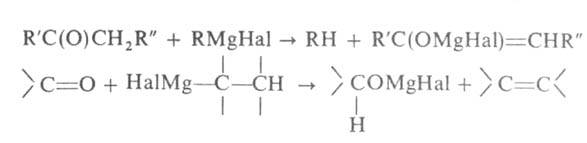
Первая р-ция может происходить, если в карбонильном соед. имеется хотя
бы один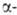 атом
Н, вторая-когда у R в реактиве Гриньяра имеется атом Н в
атом
Н, вторая-когда у R в реактиве Гриньяра имеется атом Н в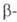 положении.
Образующийся алкоголят, подобно алкоголятам А1 (см. Меервейна-Понндорфа-Верлея реакция
), может реагировать как восстановитель, напр.: RRCH(OMgHal)
+ RCHO -> R2CO + RCH2OH Следствием енолизации м.
б. конденсация, подобная аль-дольно-кротоновой или Клайзена, напр.:
положении.
Образующийся алкоголят, подобно алкоголятам А1 (см. Меервейна-Понндорфа-Верлея реакция
), может реагировать как восстановитель, напр.: RRCH(OMgHal)
+ RCHO -> R2CO + RCH2OH Следствием енолизации м.
б. конденсация, подобная аль-дольно-кротоновой или Клайзена, напр.:
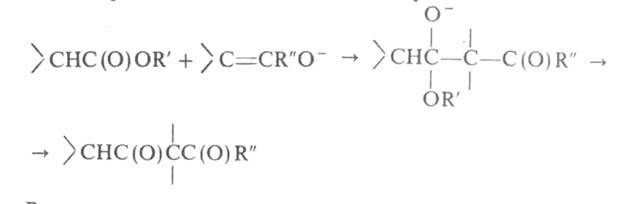
Р-ции с ароматич. кетонами часто сопровождаются образованием пинаконов.
В р-циях с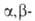 непредельными
карбонильными соед. возможно как 1,2-, так и 1,4-присоединение, а с ароматич.
производными-и 1,6-присоединение:
непредельными
карбонильными соед. возможно как 1,2-, так и 1,4-присоединение, а с ароматич.
производными-и 1,6-присоединение:
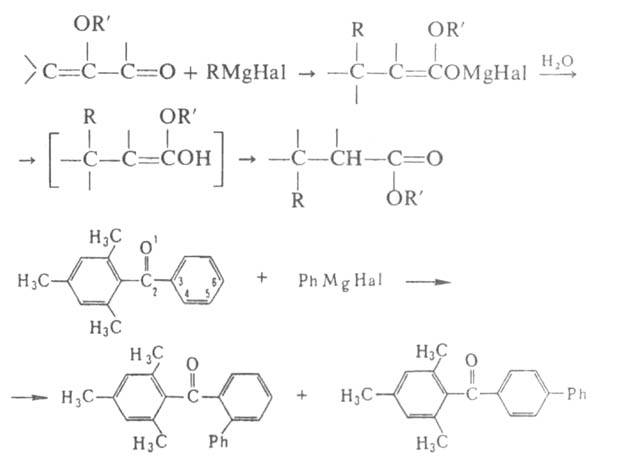
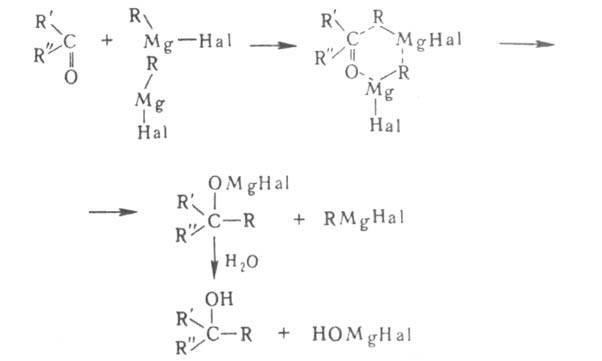
Наиб. вероятный механизм р-ции с карбонильными соед.-гетеролитический.
Предполагается, что переходное состояние представляет собой квазишестичленный
цикл:
Г. р. нашла широкое применение для синтеза элементоорг. соед., напр.:
RMgBr + HgBr, -> RHgBr + MgBr, RMgCl + AsCl3 - R3As
+ MgCl2 Взаимод. RMgHal с О2 получают пероксиды и
спирты, с HaL-алкилгалогениды, с S-сульфиды и тиолы, с Н2О -
углеводороды.
Г. р.-один из наиб. универсальных методов синтеза орг. в-в. Реактивы
Гриньяра используют также в аналит. химии, напр. для анализа в-в с подвижным
атомом Н (см. Церевитинова метод
). Синтез орг. соед. с использованием
алкенил- и алкинилмагнийгалогенидов наз. соотв. р-цией Нормана и р-цией
Иоцича.
Реактив Гриньяра впервые применил Ф. Барбье в 1899. В. Гриньяр в 1900
усовершенствовал метод, разделив р-цию на две самостоят. стадии: получение
RMgHal и его взаимод. с др. реагентом.
Лит. Иоффе СТ.. Несмеянов А. Н., в кн.: Метолы элементоорганической
химии. Магний. Бериллий. Кальций. Стронций. Барий, под общ. ред. А. Н.
Несмеянова и К. А. Кочешкова. М.. 1963, гл. 1, 2 и 4; Реакции металлоорганических
соединений как редокс-процессы. М.. 1981; Kharasch M., Reinmuth О., Grignard
reactions of nonmetallic substances, N. Y4 1954. Г. А. Артамкина.

