ИМИНОЭФИРЫ
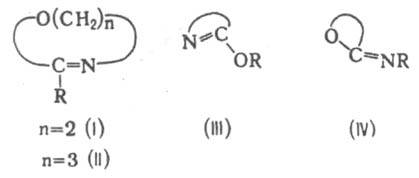
(имидаты), соед. общей ф-лы RC(=NR)OR:, где R и R - H, Alk, Ar; R: - Alk, Аr; эфиры имидовых к-т (имидокислот) RC(=NR)OH - неустойчивых изомеров первичных или вторичных амидов карбоновых к-т. Известны также И., в к-рых фрагмент —О—C=N— входит в цикл полностью [напр., D2-оксазолины (ф-ла I) и 5,6-дигидро-1,3-оксазины (II)] или частично [эфиры лактимов (III), иминолактоны (IV)].
При нагр. О-арилсодержащие И. перегруппировываются в N-ариламиды (перегруппировка Чепмена):
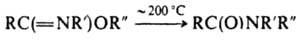
В случае R: = Alk такая перегруппировка катализируется алкилгалогенидами. Протонирование, алкилирование, ацилирование, галогенирование И. обычно осуществляется по
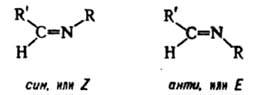
Для И. характерны два вида триадной прототропной таутомерии - имин-иминная и имин-енаминная:
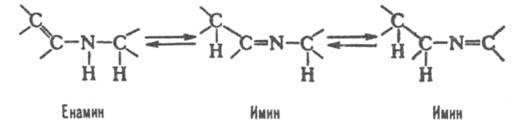
И. - основания, в безводной среде образуют с к-тами и алкилгалогенидами иминиевые соли
; в присут. водных к-т легко гидролизуются до карбонильных соед.; подобно последним вступают в конденсации типа альдолъной и кротоновой; обменивают группу NR при р-ции с аминами; присоединяют соед. с подвижным атомом водорода, а также реактивы Гриньяра; гидрируются до вторичных аминов; окисляются в амиды.
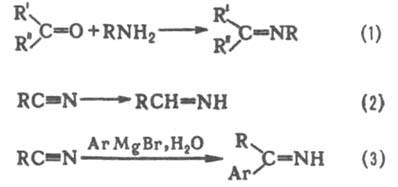
Получают И. конденсацией альдегидов или кетонов с аминами (в случае арилкетонов требуется применение кислотного катализатора, р-ция 1); восстановлением нитрилов комплексными гидридами (напр., триэтоксиалюмогидридом Na, р-ция 2), р-цией нитрилов с металлоорг. соед. (3), а также Хёша [Хеша] реакцией
, Штаудингера реакцией
, Штиглица реакцией
:
И. находят широкое применение в орг. синтезе, особенно в синтезе гетероциклов.
Иногда И. называют гетероциклич. амины с группой NH в цикле, напр., этиленимин, триэтиленимин, гексаметиленимин. См. также Шиффовы основания
.
Лит.: Общая органическая химия, пер. с англ., т. 3, М., 1982, с. 476-727.
|

