ИНДИЙ
[назван по синей (цвета индиго) линии спектра; лат. Indium] In, хим. элемент III гр. периодич. системы; ат. н. 49, ат.м. 114,82. Прир. И. состоит из двух изотопов 115In (95,7%) и 113In (4,3%). Первый слабо радиоактивен (b-излучатель, T1/25.1014 лет). Конфигурация внеш. электронной оболочки 5s25p1; степень окисления +3, редко +1; энергия ионизации In0 : In1+ : In2+ : In3+ соотв. равна 5,786390, 18,8700 и 28,03 эВ; электроотрицательность по Полингу 1,8; атомный радиус 0,166 нм, ионные радиусы (в скобках указано координац. число) для In3+ 0,076 нм (4), 0,094 нм (6), 0,106 нм (8).
И. относится к рассеянным элементам. Содержание его в земной коре 10-5 % по массе, в воде морей и океанов менее 0,02 мг/л. Известно 5 минералов - самородный И., индит FeIn2S4, рокезит CuInS2, джалиндит In(ОН)3, сакуранит (Сu, Zn,Fe)3(In,Sn)S4. И. является спутником Zn, Sn, Pb, в меньшей мере - Сu и Fe. Присутствует в сфалеритах, касситеритах, галенитах, халькопиритах (10-4—10-2%), пиритах и пирротинах (до 10-3 %). Наиб. содержание И. - в высокотемпературных гидротермальных месторождениях касситеритсульфидного и олово-сульфосольного типов. Извлекается И. из руд свинцово-цинковых, медно-колчеданных и колчеданно-полиметаллич. месторождений. Мировые ресурсы ок. 3100 т, в т.ч. промышленные 1550 т.
Свойства. И. - серебристо-белый металл; кристаллич. решетка тетрагональная, а = 0,32512 нм, с = 0,49467 нм, z = 2, пространств. группа I4/ттт. Т. пл. 156,78 °С, т. кип. 2024 °С; плотн: 7,31, жидкого И. 7,03 г/см3 (160 °C); C0p 26,7 Дж/(моль.К); DH0пл 3,26 кДж/молъ, DH0исп 237,4 кДж/моль; S0298 57,86 Дж/(моль.К); ур-ние температурной зависимости давления пара: lgp(в гПа) = 9,454 - 12593Т-1 - 0,1901gT + 1,320.10-3T (82 - 430 К), lgp(в гПа) = 9,076 - 12216T-1 + 0,2161gT(430 -2285 К); температурный коэф. линейного и объемного расширения соотв. 30,0.10-6K-1 (293-333 К) и 101.10-6 К-1 (298-323 К); теплопроводность 87,0 Вт/(м.К) при 273 К; т-ра перехода в сверхпроводящее состояние 3,405 К; r ~ 10-7 Ом.м, температурный коэф. r 4,9.10-3 К-1 (273-373 К); диамагнитен, магн. восприимчивость — 0,56.10-9. Очень мягок и пластичен; твердость по Моосу ~ 1, по Бринеллю 8,8-10,0 МПа; модуль упругости 11 ГПа; sраст 2,9-3,9 МПа.
Стандартный электродный потенциал для In0/In3+ —0,34 В. И. устойчив на воздухе, но выше ~ 800 °С горит фиолетово-синим пламенем с образованием In2О3 (см. Индия оксиды
). В воде в присут. воздуха постепенно корродирует. Медленно реагирует с минер. к-тами (легче всего с HNO3) и орг. к-тами. Взаимод. с Сl2 и Вr2, при нагр. с I2, при сплавлении с халькогенами. Не взаимод. с N2, H2, NH3, В, С. Важнейшим соед. И. посвящены отдельные статьи (см. Индия антимонид
, Индия арсенид
, Индия фосфид
). Ниже приводятся сведения о др. соединениях И.
Сульфат In2(SO4)3 светло-серые кристаллы с моноклинной решеткой; плотн. 3,44 г/см3, выше 600 °С разлагается до In2О3; гигроскопичен; раств. в воде (54% по массе при 20 °С), в водных р-рах гидролизован; из р-ров кристаллизуется при комнатной т-ре в виде пента- и декагидратов, к-рые обезвоживаются при ~ 200 °С. При действии этанола, р-ров щелочи или NH3 (рН 2-3) на водные р-ры сульфата И. выпадает осадок гидроксисульфата In(OH)SO4.2H2O. В присут. избытка сульфат-иона образуются комплексные ионы [In(SO4)2] и [In(SO4)3]3 , соответствующие им гидросульфаты кристаллизуются из р-ров, содержащих H2SO4.
Нитрат In(NO3)3.4,5H2O - расплывающиеся на воздухе кристаллы; т. пл. 74 °С; при 100-160 °С разлагается до
оксинитрата InONO3, при 230-250 °С - до In2О3; хорошо раств. в воде и этаноле. Получают взаимод. металла с HNO3. Используют для получения In2О3 и др. соединений И.
Ортофосфат InРО4 - кристаллы с ромбич. решеткой; т.пл. 1600°С; выше 1800°С разлагается; плотн. 3,91 г/см3; не раств. в воде; разлагается р-рами щелочей и конц. минер. к-тами. Получают в виде дигидрата (к-рый обезвоживается выше 300 °С) при действии Н3РО4 на р-ры солей И. Используют как добавку к шихте при произ-ве спец. стекол и к зубным цементам.
Св-ва важнейших галогенидов И. приведены в табл. 1.
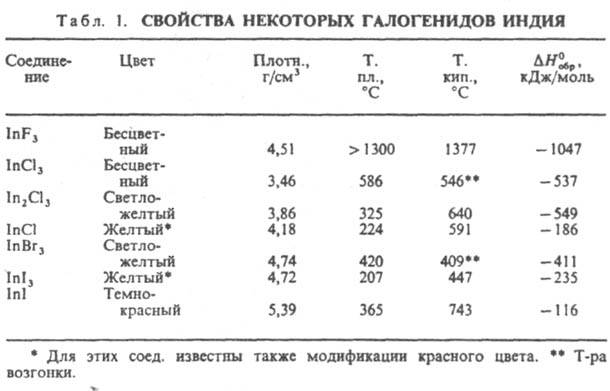
Безводный трифторид InF3 не раств. в воде; получают его фторированием И., тригидрат InF3.3H2O - взаимод. оксида или гидроксида И. с фтористоводородной к-той. Тригидрат при нагр. разлагается с образованием оксифторида InOF; раств. в воде (5,8% по массе при 25 °С); разлагается при действии минер. к-т и щелочей. Безводный трихлорид InСl3 очень гигроскопичен, расплывается на воздухе; раств. в воде (63% по массе при 20 °С), этаноле, диэтиловом эфире, ацетоне; получают хлорированием металла при незначит. нагревании. Кристаллизуется из водных р-ров в виде тетрагидрата InСl3.4Н2О с т. пл. 56 °С; при более высоких т-рах разлагается с образованием нерастворимого в воде оксихлорида InOCl. При сплавлении безводного InСl3 с металлич. И. можно получить монохлорид, а также ряд промежут. хлоридов - In3Cl4, In2Cl3 и др. Они представляют собой комплексные соед., напр., сесквихлорид In2Сl3 имеет строение In3I [InIII Сl6]. Все они гигроскопичны, при действии воды диспропорционируют на металлич. И. и InСl3. Хлориды И. - промежут. продукты при получении И. высокой чистоты.
Трибромид и трииодид И. по св-вам напоминают InСl3, но менее реакционноспособны (особенно InI3). InBr3 получают действием паров Вr2 на нагретый металл, InI3 -сплавлением элементов. Используют их для синтеза соед. И. с полупроводниковыми св-вами. InI3 и InI - компоненты наполнителя металлогалогенных ламп. В отличие от InCl и InBr моноиодид И. негигроскопичен и при комнатной т-ре почти не взаимод. с водой. Р-римость InI в воде 4,7.10-4 моль/л. Его можно осаждать из водных р-ров, напр., при анодном растворении И.
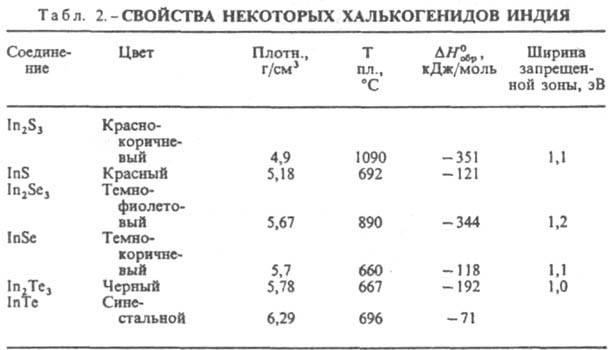
Св-ва важнейших халькогенидов И. приведены в табл. 2. Для И. характерно образование халькогенидов типов In2X, InX, In2X3, а также промежут. соед. между InX и In2Х3 и в-в с большим содержанием халькогена. Соед. In2Х метастабильны, плавятся инконгруэнтно, обладают большой летучестью; InX и In2Х3 плавятся конгруэнтно. Халькогениды InS и InSe имеют слоистую структуру типа GaS со связью металл-металл. Для InTe характерна резкая анизотропия св-в: вдоль оси кристалла он имеет металлич. проводимость, в перпендикулярном направлении - полупроводниковую. Халькогениды И. не раств. в воде, реагируют с конц. к-тами и р-рами щелочей. Обладают полупроводниковыми св-вами.
Получают халькогениды сплавлением соответствующих элементов. Соед. InX и In2Х3, как и нек-рые сложные халькогениды, напр. CuInSe2, - перспективные полупроводниковые материалы.
Соед. И. с элементами V гр. (InAs, InSb, InP) - полупроводниковые материалы.
Получение. Сырье для получения И. - отходы и промежут. продукты свинцово-цинкового и оловянного произ-в. И. выщелачивают из них серной к-той. Для отделения И. от сопутствующих металлов и концентрирования р-ров используют экстракцию, напр., р-ром ди-2-этилгексилфосфорной к-ты в керосине, или ионный обмен, напр., на фосфорнокислых катионитах.
Выделяют И. из р-ров электролизом либо цементацией на металлич. Аl (т.е. вытеснением И. из р-ра по р-ции: In3+ + Аl0 D In0 + Аl3+) с послед. переплавкой под слоем щелочи.
Для очистки И. используют чаще всего электролитич. рафинирование, вакуумную обработку для удаления летучих примесей, зонную плавку или вытягивание кристаллов из расплава. Предложен также ряд методов очистки И. с промежут. образованием его соед., в частности хлоридов.
Определение. Качественно И. может быть обнаружен по сине-фиолетовому окрашиванию пламени или спектральным методом. Предложен ряд р-ции с CsCl, фторидом, тиоцианатом, оксалатом аммония, акридином, 8-гидроксихинолином и др., а также ряд цветных р-ций с ализарином, морином, алюминоном и др. реагентами. Эти хим. р-ции малоспецифичны и требуют предварит. отделения И. от большинства др. элементов.
Для количеств. определения И. применяют комплексонометрию, а также амперометрич. титрование с K4[Fe(CN)6]. Гравиметрич. методом И. определяют в виде In2O3, In2S3, 8-гидроксихинолината. Для определения малых кол-в И. используют радиоактивац., спектральный, полярографич. методы. Предварительно производится концентрирование И. методами экстракции, электролиза или соосаждения.
Применение. И. легирующая добавка к полупроводниковым Ge и Si; герметизирующий материал в вакуумных приборах и космич. аппаратах; материал для соединения пьезоэлектрич. кристаллов. Его используют также для нанесения покрытий на пов-сть подшипников, зеркал и рефлекторов, как компонент легкоплавких сплавов, применяемых в качестве припоев, в термоограничителях, предохранителях, сигнальных устройствах, в радиац. контурах ядерных реакторов.
Мировое произв-во И. (без СССР) ок. 60 т/год (1984). Осн. производители - Япония, Канада, США, Бельгия, Перу.
И. токсичен; ПДК 0,1 мг/м3 (в США). Пыль И. и его соед. может вызвать воспалит. и склеротич. поражения легких, вредно действует на печень и селезенку. Р-римые соед. И. раздражают кожу, глаза, слизистые оболочки. По нек-рым данным, И. малотоксичен при введении в желудок и внутривенно.
И. открыт Ф Рейхом и И. Рихтером в 1863.
Лит.: Федоров П. И., Мохосоев М. В., Алексеев Ф. П., Химия галлия, индия и таллия, Новосиб., 1977; Химия и технология редких и рассеянных элементов, под ред. К. А. Большакова, т. 1, М., 1976, с. 281-325; Шека З. А., Шека И. А., Галогениды индия и их координационные соединения, К., 1981; Смирнов В. А., Дмитриев B. C., Редькин А. Н., Химия одновалентного индия, М., 1986; Яценко С .П., Индий: свойства и применение, М., 1987.
П. И. Федоров.
|

