ИОДБЕНЗОЛ
(фенилиодид) С6Н5I, мол. м. 204,02; бесцв. жидкость с эфирным запахом; т. пл. -31.3 °С, т. кип. 188,4°C; плотн. 1,8307 г/см3 (20°С), 1,861 г/см3 (0°С); nD20 1,6204; давление пара (в кПа): 1,06 (63 °С), 2,66 (79,6 °С), 4,60 (98 °C); g 38,3.10-3 Н/м (25°С); m 5,7.10-30 Кл.м (в парах), 4,6.10-30 Кл.м (в бензольном р-ре); С0p 112,3 Дж/(моль.К) (-47°С); DH0пл 8,76 кДж/моль, DH0исп 40 кДж/моль.
Р-римость в воде 0,34 г/л (30 °С); хорошо раств. в орг. р-рителях. Образует азеотропные смеси с фенолом (53% И., т. кип. 177,7°С), п-крезолом (88% И., т. кип. 187,9°С), этиленгликолем (76% И., 170,2°С)и др.
Электроф. замещение в И. происходит с образованием преим. пара-
и орто
-производных. При действии на И. жидкого Сl2 на солнечном свету образуются производные от n-хлориодбензола до пентахлориодбензола. Нагревание с I2 в ледяной уксусной к-те при одновременной обработке SO2 и дымящей HNO3 или NaNO2 и дымящей H2SO4 при 200 °С приводит к n-дииодбензолу. При нитровании HNO3 образуются п- и о-нитроиодбензолы (59 и 41% соотв.), при взаимод. с хлорсульфоновой к-той при 0 °С - n,n-дииоддифенилсульфон, с H2SO4 - n-иодбензолсульфокислота. И. - арилирующий агент; реагирует с KNH2 в жидком NH3 с образованием анилина, дифенил- и трифениламинов; с водяным паром в присут. активированной H2SiO3 (380 °С) образует фенол, с KCN - бензонитрил. Легко окисляется Н2О2 или надсерной к-той до иодозобензола С6Н5IO, озоном или орг. пероксидами - до иодилбензола С6Н5IO2. При действии хлора в безводной среде образуется С6Н5IСl2. Восстанавливается электролитически в спиртовом р-ре NaOH при 70 °С в бензол.
И. получают иодированием бензола в присут. окислителей, необходимых для связывания HI, напр. в среде ледяной уксусной к-ты в присут. НNО3 и H2SO4 выход И. 80%. Известны иодирование бензола в среде ССl4 системой I2-C6H5I-(OCOCF3)2 при 20°С (выход И. 72%), иодом в присут. SbCl5 или тетрафторбората нитрония, а также через таллийорг. соед. (выход 96%):
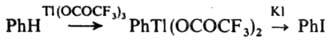
Чистый И. получают диазотированием анилина с послед. разложением образовавшегося фенилдиазонийхлорида в присут. KI. И. обладает местным раздражающим действием.
Лит.: Меркушев Е. Б., "Успехи химии", 1984, т. 53, в. 4, с. 583-94.
Г. В. Моцарев.
|

