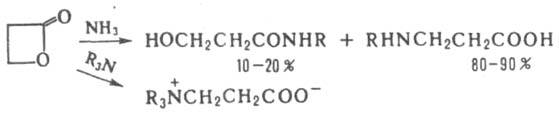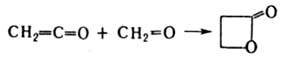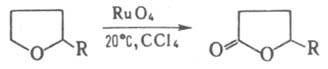ЛАКТОНЫ
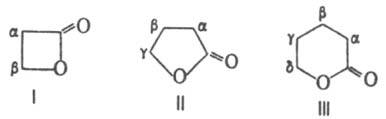
, внутренние сложные эфиры гидроксикислот. В зависимости от числа атомов в цикле различают b-Л. (4 атома), g-Л. (5 атомов) и т. д. По номенклатуре ИЮПАК, Л., образованные из алифатич. к-т, называют, добавляя окончание "олид" к назв. соединения-основы; место замыкания цикла указывают цифрой (начало нумерации - карбоксильный атом С). Допускаются также наименования, основанные на тривиальных назв. карбоновых к-т с тем же числом атомов С. В этом случае место замыкания цикла указывается греч. буквой. Так, соед. I наз. 3-пропанолид, или b-пропиолактон, соед. II - 4-бутанолид, или g-бутиролактон, соед. III-5-пентанолид, или d-валеролактон.
М.б. также использованы тривиальные и систематич. назв., принятые для гетероциклич. соед., напр. тетрагидро-2-фуранон
для соед. II. Л., содержащие в цикле более 8 атомов, относятся к макролидам.
Л.-жидкости или легкоплавкие твердые в-ва, хорошо раств. в полярных орг. р-рителях и в воде (см. табл.). Низшие Л.-лакриматоры.
СВОЙСТВА ЛАКТОНОВ
|
|
|
|
|
|
|
|
|
|
Соединение
|
Т. пл., °С
|
Т. кип., °С/мм рт. ст.
|
d420
|
nD20
|
|
|
|
b-Пропиолактон
|
-31,2
|
155/760 51/10
|
1,1460
|
1,4131
|
|
|
|
g-Бутиролактон
|
-43,5
|
206/760 90/20
|
1,1299
|
1,4353
|
|
|
|
d-Валеролактон
|
-12,5
|
299/760
97/4
|
1,0794
|
1,4574
|
|
|
|
g-Валеролактон
|
-36,0
|
207/760 84/12
|
1,0526
|
1.4322
|
|
|
|
e-Капролактон
|
-5,0
|
98-99/2
|
1.0693
|
1.4611*
|
|
|
|
|
|
|
|
|
|
* При 22 °С.
По хим. св-вам Л. - эфиры сложные
. При нагр. с р-рами щелочей, а в нек-рых случаях с водой, гидролизуются с образованием соответствующих гидроксикислот. наиб. устойчивы к гидролизу g-Л.
Под действием разл. восстановителей Л. превращ. в карбоновые к-ты, диолы, лактолы (ф-ла IV) или простые циклич. эфиры енолов:
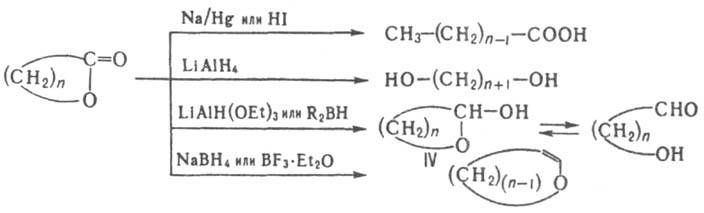
Все Л., за исключением g-Л. легко полимеризуются в присут. катионных и анионных катализаторов с образованием полиэфиров общей ф-лы [—OCHR:(CRR)nCO—]m, где R, R, R: - H, Alk или др.
С гидразином и фенилгидразином Л. дают соответствующие гидразиды и фенилгидразиды гидроксикислот. С ароматич. соед. в присут. АlСl3 образуют w - арилзамещенные карбоновых к-т:
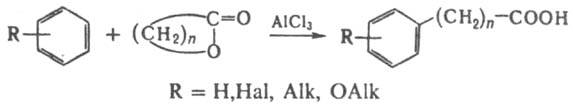
С нуклеоф. агентами Л. реагируют с раскрытием цикла, напр.:
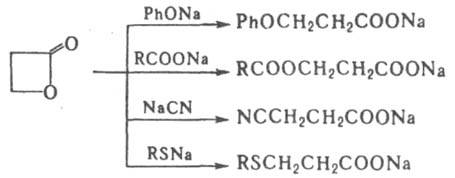
Р-ции g- и d - Л. осуществляются в более жестких условиях, чем р-ции b-Л. Протонные к-ты и к-ты Льюиса значительно ускоряют эти р-ции.
С NH3, первичными, вторичными алифатич. аминами, замещенными анилинами b-Л. образуют смесь амидов b-гидроксикислот и b-аминокислот, с третичными аминами - бетаины, напр.:
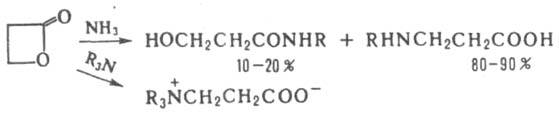
В р-циях с NH3 и первичными аминами g-Л. образуют амиды g-гидроксимасляной к-ты, к-рые при нагр. выше 180 °С отщепляют воду, превращаясь в 2-пирролидон или его N-замещенные производные; с алифатич. и ароматич. вторичными аминами g- и d-Л. дают гидроксиамиды и производные аминокислот, напр.:
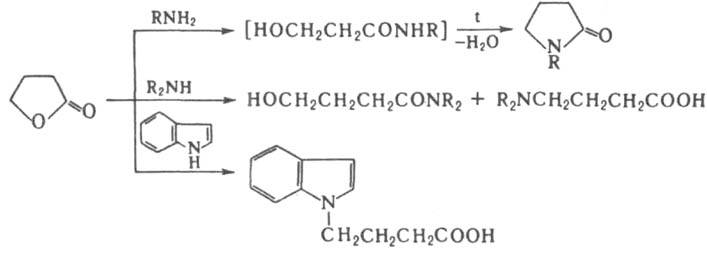
Направление алкоголиза Л. зависит от рН среды: в кислых средах образуются алкоксикислоты, в щелочных - сложные эфиры гидроксикислот, напр.:
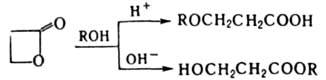
Для b-Л. характерен пиролиз с образованием олефина и СО2. Остальные Л. термически стабильны и лишь выше 500 °С изомеризуются в непредельные к-ты.
Осн. методы получения Л. - циклизация соответствующих гидрокси- и галогенокислот:
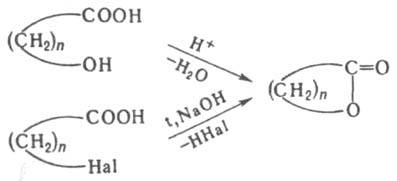
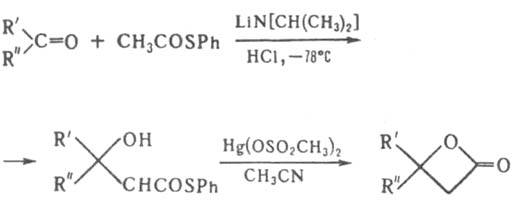
b-Л. получают из гидроксикислот под действием сильных дегидратирующих агентов, напр. дициклогексилкарбодиимида, или по р-ции кетенов с карбонильными соед., напр.:
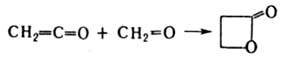
Их также синтезируют циклизацией фенилтиоэфиров b-гидроксикислот в присут. солей Hg:
g- и d-Л. легко образуются при подкислении водных р-ров гидроксикислот или при перегонке галогенокислот. Они также м.б. получены окислением циклич. кетонов надкислотами (см. !b БAЙEP BИЛЛИГEP PEAKЦ>Байера-Виллигера реакция
).
d-Л. также получают сухой перегонкой солей d-галогенокислот.
Л. могут быть также синтезированы окислением производных ТГФ по р-ции:
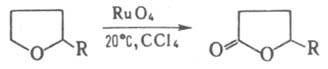
Л. содержатся в молоке и молочных продуктах, в растительных мускусах (см. Мускусы
). Нек-рые Л. - исходные в-ва в биосинтезе терпенов (напр., мевалолактон), в синтезе биологически инертных гидрофильных полиуретанов, используемых в хирургии; входят в состав теплочувствительных материалов, применяемых в копировальной технике.
Лит.: Общая органическая химия, пер. с англ., т. 4, М., 1983; Rodds chemistry of carbon compounds, 2 ed., ed. by S. Cofley, v. 1, pt D, Amst., 1965, p. 99 113; Knight D. W., в кн.: General and synthetic methods, v. 4, U 1981, p. 87-137; v. 5, L, 1982, p. 100-47; Annual reports in organic synthesis, 1970 1983, ed. by L.G. Wade, M.J. ODonnell. N.Y., 1971-84. A.M.Сахаров
.