ЛИПИДЫ
(от греч. lipos - жир), жироподобные в-ва, входящие в состав всех живых клеток. Определение понятия липидов неоднозначно. Иногда к Л. относят любые прир. в-ва, извлекаемые из организмов, тканей или клеток такими неполярными орг. р-рителями, как хлороформ, диэтиловый эфир или бензол. В нек-рых случаях Л. рассматривают как производные жирных к-т и родственных им соед. или как любые прир. амфифильные в-ва (их молекулы содержат как гидрофильные, так и гидрофобные группировки). Ни одно из этих определений не является исчерпывающим. Следует ли причислять к Л. терпеноиды, жирорастворимые витамины и гормоны, остается спорным.
Исторический очерк. Нек-рые Л. (жиры животные
, растительные масла
) используют с древнейших времен как продукты питания, для приготовления лек. и косметич. препаратов, лакокрасочных материалов, а также для освещения. С нач. 18 в. Л. стали использовать для мыловарения, а в 20 в. - для приготовления моющих ср-в, эмульгаторов, детергентов, пластификаторов и технол. смазок. Первый элементный анализ Л. выполнен в нач. 19 в. А. Лавуазье, а первые исследования по выяснению хим. строения Л. принадлежат К. Шееле и М. Шеврёлю [Шеврелю]. Впервые синтезы триглицеридов осуществили М. Бертло в 1854 и Ш. Вюрц в 1859. Фосфолипиды выделены М. Гобли в 1847, а затем получены в более чистом виде Ф. А. Хоппе-Зейлером в 1877. К этому времени уже было установлено строение ряда важнейших жирных к-т.
Дальнейшую историю изучения Л. можно разделить на три периода, различающиеся по методич. уровню исследований. На первом этапе (1880-1950) Л. исследовали традиционными методами орг. химии, второй этап (1950-1970) характеризуется широким применением методов хроматографии, а последний (70-80-е гг.) - использованием таких физ.-хим. методов, как масс-спектрометрия, оптич. спектроскопия и радиоспектроскопия, флуоресцентный анализ и др.
Классификация Л. В соответствии с хим. строением различают три осн. группы Л.: 1) жирные к-ты и продукты их ферментативного окисления, 2) глицеролипиды (содержат в молекуле остаток глицерина), 3) Л., не содержащие в молекуле остаток глицерина (за исключением соед., входящих в первую группу). В первую группу входят наряду с жирными к-тами простагландины
и др. гидроксикислоты; во вторую - моно-, ди- и триглицериды и их алкил- и 1-алкенил (плазмалогены
)замещенные аналоги, а также гликозилдиглицериды
и большинство фосфолипидов
; в третью группу входят сфинголипиды
, стерины
и воски
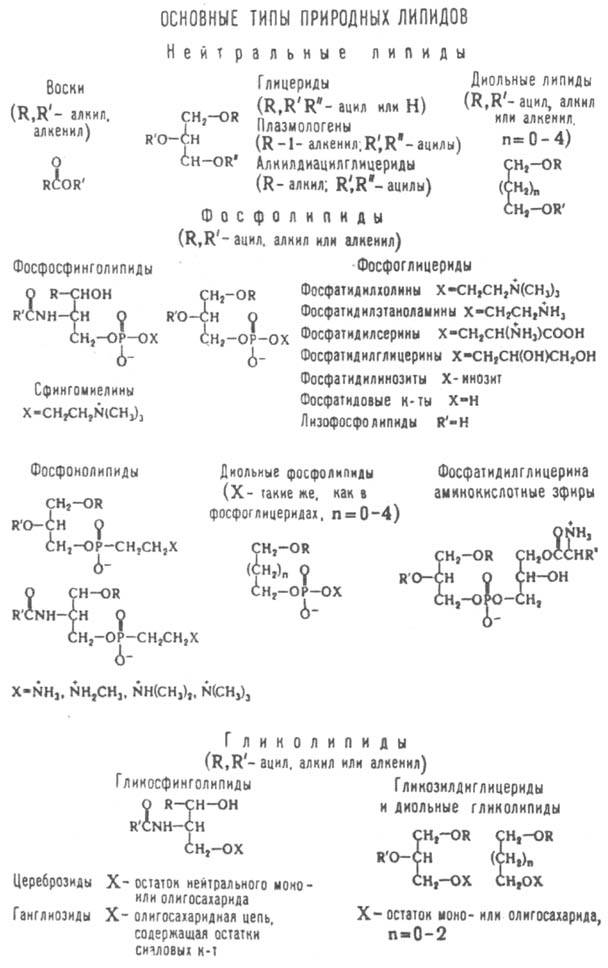
. По др. классификации (она приведена на схеме), Л. подразделяют на нейтральные Л., фосфолипиды и гликолипиды. В организмах встречаются также многочисл. типы минорных Л. - фосфатидилглицерин
, липопептиды
, липополисахариды
, диольные липиды
и др. В липидных экстрактах часто присутствуют продукты частичного гидролиза Л. - лизофосфолипиды
и своб. жирные к-ты, а также продукты автоокисления и ферментативного окисления последних, в т.ч. разнообразные продукты превращ. арахидоновой к-ты - т. наз. эйкозаноиды
(простагландины, лепкотриены и др.).
Структура. Наиб. распространенные типы Л. - глицеролипиды и производные сфингозина СН3(СН2)12СН=CHCH(OH)CH(NH2)CH2OH. В нейтральных глицеролипидах гидроксильные группы глицерина замещены остатками жирных к-т, алифатич. спиртов или альдегидов. В полярных глицеролипидах две гидроксильные группы глицерина замещены чаще всего жирными к-тами, а третья связана
либо с остатком ортофосфорной к-ты (свободной или этерифицированной холимом, этаноламином, серином, глицерином или миоинозитом), либо с остатками сахаров, как у гликозиллиглицеридов.
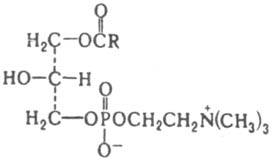
Положение заместителей в молекуле
глицерина обозначают по т. наз. системе стереоспецифич. нумераций: если в фишеровской проекции вторичная гидроксигруппа глицеринового остатка находится слева, то углеродным атомам, расположенным выше и ниже этой группы, присваивают соотв. номера 1 и 3, снабдив их индексом sn (напр., sn-1-ацил-3-глицерофосфохолин, см. ф-лу). Наряду с диацилглицерофосфолипидами распространены глицсрофосфолипиды, содержащие в положении sn-1-алкильные или 1-алкенильные заместители.
В водных средах Л. образуют бислойные, гексагональные или мицеллярные структуры. В бислоях (см. Липидный бислой
) насыщ. углеводородные цепи Л., как правило, находятся в зигзагообразной конформации и расположены параллельно друг другу.
Ось sn-1-ацильной
цепи совпадает с осью глицеринового остатка, тогда как sn-2-цепь на начальном СО—СН2-участке отходит от глицеринового остатка под прямым углом и, резко изгибаясь у a-углеродного атома, становится далее параллельной sn-1-цепи. Ненасыщ. углеводородные цепи Л. содержат одну
или неск. этиленовых связей, к-рые, как правило, имеют цис
-конфигурацию. При наличии двойных связей зигзагообразная конформация нарушается. В молекулах цвиттерионных фосфолипидов (напр., фосфатидилхолина и фосфатидилэтаноламина) полярная группировка ("головка") расположена перпендикулярно осям ацильных цепей, а в молекулах отрицательно заряженных фосфолипидов (напр., фосфатидилсерина) полярные головки направлены параллельно оси ацильных цепей. У фосфосфинголипидов оси ацильных цепей и сфингозинового остатка также расположены параллельно друг другу. В случае сфингомиелина амидная группа, соединяющая эти остатки, расположена перпендикулярно к ним, а жирно-кислотная цепь изгибается у a-углеродного атома, подобно sn-2-цепи фосфоглицеридов. Иную пространственную структуру имеют гликосфинголипиды. У цереброзидов параллельное расположение алифатич. цепей обеспечивается в результате изгибов цепи сфингозина при первом и шестом атомах С, а кольцо остатка моносахарида ориентировано почти перпендикулярно к углеводородным цепям. У гликосфинголипидов с олигосахаридной цепью последняя ориентирована преим. по направлению осей углеводородных цепей.
Получение Л. Прир. Л. выделяют из животных или микробных источников, комбинируя экстракцию орг. р-рителями с хроматографич. методами очистки. При этом отдельные группы Л. получают в виде смеси однотипных в-в, имеющих одинаковые полярные головки, но различающихся по длине и степени ненасышенности алифатич. цепей. Широко распространены полусинтетич. методы - переацилирование прир. Л. и превращ. одних классов Л. в другие. В первом случае прир. Л., напр. фосфатидилхолины, подвергают деацилированию или ферментативному гидролизу с помощью фосфолипазы А2, а затем полученный глицерофосфохолин
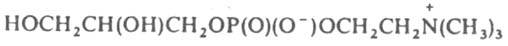 или лизофосфатидилхолин реацилируют индивидуальными жирными к-тами. При использовании для реацилирования синтетич. к-т, несущих флуоресцентные, спиновые, фотореактивные группировки или радиоактивные метки, получают липидные зонды
. Для превращ. одних групп прир. глицерофосфолипидов в другие используют реакцию трансфосфатидилирювания с помощью фосфолипазы D. Этим путем из фосфатидилхолина в присут. воды, избытка этаноламина, серина или глицерина получают соотв. фосфатидовую к-ту, фосфатидилэтаноламин, фосфатидилсерин или фосфатидилглицерин. Фосфатидовая к-та, в свою очередь, м.б. этерифицирована холином, этаноламином или серином в присут. разл. конденсирующих агентов. По др. схеме осуществляется неполный синтез сфинголипидов. Напр., для превращ. доступных сфингомиелинов в гликосфинголипиды исходный сфингомиелин гидролизуют в цсрамид CH3(CH2)12CH=CHCH(OH)CH[NH(О)CR]CH2OH, к-рый превращают в 3-О-бензоильное производное. Последнее затем гликозилируют с помощью соответствующих бромзамещенных ацетилсахаров, после чего защитные бензоильную и ацетильные группы удаляют метанолизом в щелочной среде.
Получение индивидуальных фосфолипидов и сфинголипидов обычно осуществляют полным хим. синтезом. Таким же путем получают также простагландины и др. эйкозаноиды.
или лизофосфатидилхолин реацилируют индивидуальными жирными к-тами. При использовании для реацилирования синтетич. к-т, несущих флуоресцентные, спиновые, фотореактивные группировки или радиоактивные метки, получают липидные зонды
. Для превращ. одних групп прир. глицерофосфолипидов в другие используют реакцию трансфосфатидилирювания с помощью фосфолипазы D. Этим путем из фосфатидилхолина в присут. воды, избытка этаноламина, серина или глицерина получают соотв. фосфатидовую к-ту, фосфатидилэтаноламин, фосфатидилсерин или фосфатидилглицерин. Фосфатидовая к-та, в свою очередь, м.б. этерифицирована холином, этаноламином или серином в присут. разл. конденсирующих агентов. По др. схеме осуществляется неполный синтез сфинголипидов. Напр., для превращ. доступных сфингомиелинов в гликосфинголипиды исходный сфингомиелин гидролизуют в цсрамид CH3(CH2)12CH=CHCH(OH)CH[NH(О)CR]CH2OH, к-рый превращают в 3-О-бензоильное производное. Последнее затем гликозилируют с помощью соответствующих бромзамещенных ацетилсахаров, после чего защитные бензоильную и ацетильные группы удаляют метанолизом в щелочной среде.
Получение индивидуальных фосфолипидов и сфинголипидов обычно осуществляют полным хим. синтезом. Таким же путем получают также простагландины и др. эйкозаноиды.
Биосинтез глицеролипидов и сфинголипидов. Центр. промежут. продукты биосинтеза глицеролипидов - 1,2-диглицериды и фосфатидовые к-ты. Последние образуются гл. обр. двумя путями: ацилированием sn-глицеро-3-фосфата с участием ацилкофермента А и ферментативным ацилированием дигидроксиацетонфосфата с послед. восстановлением его коферментом никотинамидадениндинуклеотидом (НАДН) с образованием лизофосфатидовой к-ты, к-рая далее ацилируется до фосфатидовой к-ты. Гидролиз последней под влиянием фосфатазы приводит к 1,2-диглицеридам, реагирующими
с ацилкоферментом А с образованием триглицеридов или с АТФ с образованием фосфатидовой к-ты. Диглицериды вступают во взаимод. с цитидинтрифосфатом, цитидиндифосфохолином или цитидиндифосфоэтаноламином, образуя соотв. фосфатидовую к-ту, фосфатидилхолин или фосфатидилэтаноламин, напр.:
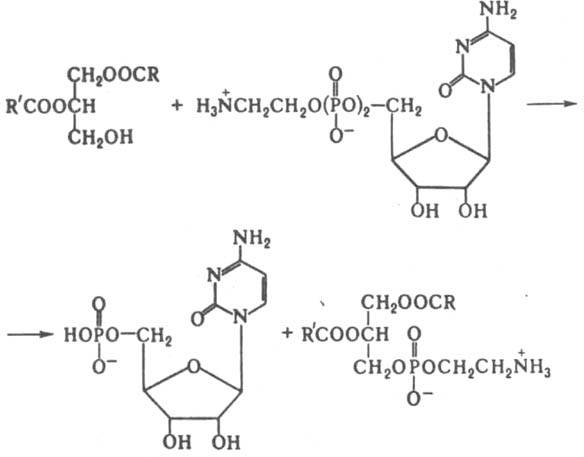
Фосфатидилэтаноламин, в свою очередь, может превращ. в фосфатидилхолин путем метилирования S-аденозилметионином
или реагировать с серином, образуя в результате переэтерификации фосфатидилсерин. У бактерий осуществляется др. путь биосинтеза фосфатидилсерина и фосфатидилэтаноламина; фосфатидовая к-та, взаимодействуя с цитидинтрифосфатом, образует цитидиндифосфодиацилглицерин, к-рый реагирует с серином, образуя фосфатидилсерин. Его декарбоксилирование приводит к фосфатидилэтаноламину, а р-ция с глицерофосфатом - к фосфатидилглицерину Последний вновь может взаимод. с цитидиндифосфодиацилглицерином, превращаясь в дифосфатидилглицерин. В биосинтезе сфинголипидов ключевое соед. - церамид, образующийся в результате N-ацилирования сфингозина ацилкоферментом А. Р-ция церамида с цитидиндифосфохолином приводит к сфингомиелину, а его взаимод. с производными уридина (уридиндифосфоглюкозой или уридиндифосфогалактозой) - к цереброзидам. Возможен и др. путь биосинтеза цереброзидов, основанный на р-ции производных уридина со сфингозиновыми основаниями с образованием психозина (галактозид сфингозина) и его последующем N-ацилировании ацилкоферментами А. Из цереброзидов путем последоват. присоединения остатков моносахаридов и сиаловой к-ты под влиянием соответствующих гликозилтрансфераз образуются гликосфинголипиды с более длинными сахарными цепями.
Биологические функции Л. В полной мере биол. роль Л. еще не выяснена. Нейтральные Л. (жиры) представляют собой форму депонирования метаболич. энергии. Фосфолипиды, гликолипиды и стерины - структурные компоненты мембран биологических
; оказывают влияние на множество мембранных процессов, в т. ч. на транспорт ионов и метаболитов, активность мембраносвязанных ферментов, межклеточные взаимод. и рецепцию. Нек-рые гликолипиды -рецепторы или корецепторы гормонов, токсинов, вирусов и др. Фосфатидилинозиты участвуют в передаче биол. сигналов. Эйкозаноиды - высокоактивные внутриклеточные регуляторы, межклеточные медиаторы и иммуномодуляторы, участвующие в развитии защитных р-ций и воспалит. процессов.
Лит.: Кейтс М., Техника липидологии, пер. с англ., М., 1975; Крепc Е. М., Липиды клеточных мембран. Л., 1981; Химия липидов, М., 1983; Препаративная биохимия липидов, под ред. Л. Д. Бергельсона, М., 1981.
Л. Д. Бергельсон.
|

