МИНЕРАЛ
(от позднелат.
minera-руда), прир. твердое тело с характерными хим. составом, кристаллич. структурой
и св-вами. Образуется в результате физ. и хим. процессов (экзогенных, эндогенных
и метаморфических; см. Полезные ископаемые
)в глубинах и на пов-сти Земли,
Луны, др. планет и космич. тел. М.-составная часть горных пород, руд и метеоритов.
Как исключение к М. относят жидкую ртуть и прир.
амальгамы, аморфные опал и аллофан (водный силикат алюминия). Выделяют также
метамиктные М., к-рые утратили кристаллич. строение в результате радиоактивного
распада. М., как правило,-неорг. в-ва, но иногда к ним относят кристаллич. орг.
соединения (в частности, окса-латы), нек-рые твердые углеводороды и ископаемые
смолы (компоненты янтаря). Воду, в отличие от льда, обычно не считают М. По
мнению В. И. Вернадского, однако, М. являются не только твердые прир. образования,
но также жидкости и газы.
Понятие М. употребляют
для обозначения минеральных индивида, вида и разновидности. Минер. индивиды-отдельные
кристаллы или кристаллич. зерна. Их размеры варьируют от 1-100 нм (коллоидные
М.) до неск. м. Минер. вид-совокупность минер. индивидов однотипной структуры,
хим. состав к-рых может изменяться в определенных пределах без изменения структуры.
М. одинакового состава, но разной структуры-полиморфные модификации (напр.,
алмаз и графит, кальцит и арагонит) - относят к разным минер. видам. Непрерывные
ряды твердых р-ров (изоморфные смеси) условно делят на неск. минер. видов. Так,
в двухкомпонентных твердых р-рах выделяют обычно три минер. вида (с содержанием
одного из компонентов 100-75, 75-25 и 25-0 мол. или ат. %), реже два (0-50 и
50-100 мол. или ат. %), а в трехкомпонентных-семь или три. Минер. разновидность
выделяют внутри минер. вида по особенностям структуры, состава, морфологии и
св-в. Известно ок. 3000 минер. видов и почти столько же разновидностей.
Называют М. по составу,
месту находки, особенностям морфологии, характерному св-ву, в честь ученых,
путешественников, космонавтов, политич. деятелей и т.д.
Структура. Структурными
единицами в узлах кристаллич. решетки м. б. атомы (как, напр., в алмазе), ионы
(напр., Na+, UO22+, NH+4,
Н3О+ , Cl-, CO32-, PO43-),
а также молекулы (S8 в сере, As4S4. в реальгаре).
Они удерживаются в структуре благодаря ионной, ковалентной, металлич. и водородной
связям, а также ван-дер-ваальсовым взаимодействиям. В т. наз. гомо(изо)десмич.
структурах имеется только один тип связи (ковалентная в алмазе, ионная в галите,
металлическая в золоте); но гораздо чаще встречаются гетеро(анизо)десмич. структуры
с неск. типами связи. Пространств. расположение структурных единиц, связанных
наиб. прочными связями, определяет геом. "мотив" структуры: островной
(в т.ч. кольцевой), цепочечный, ленточный, слоистый, каркасный, координационный.
В структуре каждого М. выделяют элементарную ячейку с соответствующей симметрией
и параметрами (см. Кристаллы
).
Реальная структура М. отличается
от идеальной наличием дефектов (вакансии в отдельных узлах кристаллич. решетки,
примесные атомы или ионы в узлах или между узлами, изменение валентности у части
ионов) и дислокаций. Упорядочение вакансий может приводить к увеличению одного
из параметров элементарной ячейки. Для слоистых М. (слюды, графит, молибденит
и др.) характерна политипия, при к-рой происходит небольшой сдвиг слоев (пакетов)
относительно друг друга с изменением периодичности в их чередовании. В результате
разл. политипы одного М. отличаются друг от друга параметрами вдоль одной из
осей (причем эти параметры кратны одной и той же величине). При этом может происходить
изменение вида симметрии элементарной ячейки вплоть до изменения сингонии. Однако
существ. перестройки структуры, как при полиморфизме, не происходит.
Кроме того, атомы или ионы
в нек-рых М. могут распределяться по узлам кристаллич. решетки закономерно или
статистически; соответственно различают упорядоченные и неупорядоченные структуры.
Химический состав и
формулы. В состав М. входят все стабильные и долгоживущие изотопы элементов
периодич. системы, кроме инертных газов (хотя Аr и Не могут накапливаться в
М. как продукты радиоактивного распада). Различают видообразующие элементы и
элементы-примеси, содержание к-рых в М. составляет соотв. единицы-десятки и
единицы-доли процента по массе. К последним обычно относят редкие и рассеянные
элементы: Rb, Cs, Ra, Sc, Ga, In, Tl, Ge, Hf, Th, РЗЭ, Re, I, Br и др., к-рые,
как правило, не образуют самостоятельных М. Примеси м. б. структурными (изоморфными)
или механическими (адсорбир. элементы и соед., газово-жидкие микровключения,
микроскопич. и суб-микроскопич. включения др. М.), что связано с условиями образования
М. и с особенностями его кристаллич. структуры.
По числу (один, два или
больше) видообразующих элементов среди М. выделяют соотв. простые в-ва, бинарные
и более сложные соединения. Бинарные соед. преобладают среди интерметаллидов
(напр., Au2Bi, Pd3Sn, Pt3Fe), карбидов, нитридов,
силицидов (Fe3C, FeSi, CrN), характерны для нек-рых халькогенидов
(PbS, NiSe, Bi2Te3, NiAs, FeSb2), простых оксидов
(MgO, Fe2O3, Al2O3, SiO2),
галогенидов (NaCl, KCl, MgF2, CaF2). К более сложным соед.
относятся нек-рые интерметаллиды (Au8PbTe, CuPt2Fe), карбиды
и фосфиды (Fe2NiP, Fe20Ni3C), большая часть
халькогенидов (Cu5FeS4, CoAsS, Ag3SbS3),
гидроксиды и сложные оксиды (АlOОН, FeCr2O4), все соли
кислородсодержащих к-т {Cas [PO4]3(F, Сl, ОН)},
часть галогенидов (NH4Cl, KMgCl3.6H2O)
и все т. наз. галогеносоли (Na[BF4], Na3 [AlF6]).
Характерная особенность силикатов, боратов и ванадатов - наличие полимерных
анионов, В силикатах в строении анионного радикала принимают участие (кроме
Si и О) Аl, В и Be.
Состав нек-рых М. относительно
постоянен (кварц, гематит и др.), однако большинство М. имеют переменный состав,
как, напр., члены изоморфных рядов в двух-, трех- и многокомпонентных системах.
Состав М. выражается хим.
ф-лой. Эмпирич. ф-ла отражает соотношения входящих в состав М. элементов, к-рые
располагаются в ней слева направо по мере увеличения номера группы в периодич.
системе, а для элементов одной группы-по мере уменьшения их порядковых номеров,
напр. кобальтин CoAsS, сподумен Li2O • Аl2О3
• 4SiO2. К р и с т а л л о х и м. ф-ла отражает связь состава со
структурой. Она записывается по определенным правилам: сначала катионы; затем
анионы, при этом комплексные анионы заключают в квадратные скобки; после аниона
т. наз. дополнит. анионы (F-, Cl-, ОН-, О2-);
молекулы воды обычно записываются в конце ф-лы; изоморфные элементы ставят в
круглые скобки через запятую. Можно указать мотив полимерного аниона: цепочечный
или ленточный (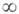 ),
слоистый (
),
слоистый (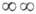 ),
каркасный (
),
каркасный (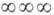 ). Напр., кристаллохим. ф-ла кобальтина имеет вид Co[AsS], сподумена-
). Напр., кристаллохим. ф-ла кобальтина имеет вид Co[AsS], сподумена-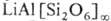 , талька-Mg3
, талька-Mg3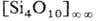 (OH)2,
альбита-
(OH)2,
альбита-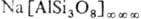 . Степень окисления указывают справа вверху от символа элемента, а координац.
число-слева вверху в круглых скобках, напр.: магнетит Fe2+Fe23+
O4, андалузит (6)Al(5)Al [SiO4]
О. Ф-лы М., для к-рых характерны разнообразные изоморфные замещения, записывают
в обобщенном виде, напр. блеклые руды М+10М22+
[Y4X13], где М+ -Сu, Ag; M2+ -Fe,
Zn, Сu, Hg, Cd, Mn; Y-As, Sb, Bi, Те; X-S, Se.
. Степень окисления указывают справа вверху от символа элемента, а координац.
число-слева вверху в круглых скобках, напр.: магнетит Fe2+Fe23+
O4, андалузит (6)Al(5)Al [SiO4]
О. Ф-лы М., для к-рых характерны разнообразные изоморфные замещения, записывают
в обобщенном виде, напр. блеклые руды М+10М22+
[Y4X13], где М+ -Сu, Ag; M2+ -Fe,
Zn, Сu, Hg, Cd, Mn; Y-As, Sb, Bi, Те; X-S, Se.
В составе М. может присутствовать
вода: связанная, или конституционная, в ионизир. виде (ОН-, Н3О+);
кристаллизационная в виде молекул Н2О, кол-во к-рых в элементарной
ячейке постоянно, и свободная (адсорбированная, капиллярная, межслоевая и др.),
кол-во к-рой непостоянно, что обозначается n.Н2О
или aq. M. может содержать одновременно неск. типов воды, что отражается в кристаллохим.
ф-лах, напр.: гипс Са [SO4]•2Н2О, гидромусковит (К, Н3O+)
Аl2 [AlSi3O10] (OH)2•nН2O.
Реальный состав М. всегда
отличается от идеальной ф-лы минер. вида. Так, ф-ла минер. вида сфалерита-ZnS,
а в результате хим. анализа конкретного образца сфалерита м. б. получена, напр.,
такая ф-ла: (Zn0,70Fe0,15Mn0,10Cd0,03In0,02)S.
Классификация. Общепринятой
классификации М. нет. Наиб. рациональной классификацией минер. видов считают
кристаллохимическую, к-рая в равной степени учитывает хим.
состав и структурные особенности М. и позволяет выявлять взаимосвязи между составом,
кристаллич. структурой, св-вами и морфологией (см. ниже) М. Так, иногда М. подразделяют
по составу на шесть типов: самородные элементы (простые в-ва), интерметаллиды,
карбиды и им подобные, халькогениды, кислородные соед., галогенные соединения.
В трех последних типах характер аниона (простой или комплексный) служит основанием
для выделения соответствующих подтипов, а конкретный состав аниона-для выделения
классов (см. табл.).
КЛАССИФИКАЦИЯ МИНЕРАЛОВ

Морфология (формы
выделения). М. часто образуют кристаллы определенной формы, свойственной данному
минер. виду. Облик их м. б. изометрический, удлиненный (столбчатый, игольчатый
и др.) или уплощенный (таблитчатый, чешуйчатый и др.). Нередко кристаллы закономерно
срастаются в виде двойников, тройников, четверников, шестсрни-ков. Незакономерные
сростки кристаллов и кристаллич. зерен образуют минер. агрегаты (друзы, щетки,
сферолиты, оолиты и др.). Морфология кристаллов и агрегатов дает информацию
об условиях образования М. и используется при их диагностике.
Свойства М. обусловлены
их кристаллич. структурой и хим. составом. Они являются основой диагностики
М., учитываются при поисках в разведке полезных ископаемых, при обогащении и
комплексной переработке руд и применении М. Мех. св-ва включают твердость, хрупкость,
ковкость, спайность, отдельность, излом, гибкость (сопротивление излому), упругость.
Под твердостью понимают степень сопротивления М. к.-л. воздействию. Для определения
относит. твердости М. используют шкалу Мооса, составленную из 10 эталонов-минералов
с условной твердостью от 1 до 10: 1-тальк, 2-гипс, 3-кальцит, 4-флюорит,
5-апатит, 6-ортоклаз, 7-кварц, 8-топаз, 9-корунд, 10-алмаз (расположены в порядке
возрастания твердости). Этими минералами царапают пов-сть исследуемого М. Т.
наз. микротвердость (кгс/мм2) рассчитывают по величине углубления,
полученного в стандартных условиях при вдавливании в М. алмазной пирамидки на
спец. приборе-микротвердомере. Твердость М. зависит гл. обр. от его кристаллич.
структуры, типа и прочности хим. связей. С твердостью М. связаны их хрупкость
и ковкость. Спайность М.-это способность раскалываться при ударе по определенным
направлениям с образованием плоских пов-стей. Спайность зависит от типа кристаллич.
решетки, прочности связей и их пространств. распределения в структуре и, в зависимости
от геом. типа структуры, может проявляться в одном, двух, трех и более направлениях.
Отдельность подобна спайности, но обусловлена двойникованием, ориентированным
замещением другими М., воздействием одностороннего давления. Излом (ступенчатый,
занозистый, раковистый, неровный) характеризует пов-сть обломков, на к-рые раскалывается
М. (не по спайности) при ударе. Упругие св-ва оценивают по характеру деформации
М. при воздействии на него мех. напряжения (см. Реология
).
О п т и ч. с в-в а М. включают
преломление, отражение и поглощение света, блеск, цвет, люминесценцию. Они также
связаны с составом и структурой М. Преломление света наблюдается у прозрачных
М. (кислородные и галогенные соед.) и характеризуется показателем преломления
п. Отражение света наблюдается в большей степени у непрозрачных и полупрозрачных
М. (металлы, интерметаллиды, халько-гениды, оксиды и гидроксиды) и характеризуется
коэф. отражения R. По величинам п и R диагностируют М.
под микроскопом в проходящем или отраженном свете. Свето-поглощение (оптич.
плотность) характеризует как прозрачные (алмаз, горный хрусталь), так и полупрозрачные
(сфалерит, сера) и непрозрачные (магнетит, золото) М. Блеск М., наблюдаемый
визуально,-одна из форм светоот-ражения. Он бывает металлическим, полуметаллическим,
алмазным, стеклянным, жирным, матовым и др. Цвет М. объясняется частичным поглощением
видимого света и обусловлен присутствием в структуре ионов-хромофоров в качестве
видообразующих элементов или изоморфных примесей, а также структурными дефектами,
газово-жидкими включениями и микроскопич. включениями окрашенных М. Нек-рые
М. способны люминесцировать при облучении, нагревании, раскалывании, в результате
трения.
Э л е к т р и ч. с в-в
а выявляются у М. при воздействии на них электркч. поля, в нек-рых случаях-при
нагр. или мех. деформации. По величине электропроводности М. делят на проводники
(металлы, интерметаллиды), полупроводники (мн. халькогениды) и диэлектрики (кислородные
и галогенные соед.). Диэлектрики не проводят электрич. тока, но на пов-сти нек-рых
из них могут возникать электрич. заряды в результате нагревания (пироэлектричество,
напр., в турмалине), давления, сжатия, растяжения (пьезоэлектричество в кварце)
и трения (трибоэлектричество).
М а г н. с в-в а проявляются
у М. в магн. поле. Они связаны с магн. моментами атомов и особенностями структуры
М. По величине магн. восприимчивости М. подразделяют на диамагнетики, парамагнетики
и ферромагнетики. По степени упорядоченности магн. моментов парамагнетики и
ферромагнетики подразделяют на антиферромагнетики (напр., ильменит, гематит),
ферромагнетики (самородное железо) и ферримагнетики (магнетит, пирротин). По
плотности (г/см3) М. делят на легкие (до 2,5), средние (2,5-4), тяжелые
(4-8) и весьма тяжелые (> 8,0). Плотность зависит от атомных масс слагающих
кристаллич. решетку атомов и ее геом. типа. Наиб. плотность (от 8 до 23 г/см3)
имеют самородные металлы. Нек-рые М. обладают радиоактивностью.
Диагностика и методы
изучения. Предварит. диагностика М. основывается на изучении морфологии
и физ. св-в М., наблюдаемых визуально. Иногда дополнительно изучают люминесцентные,
радиоактивные и магн. св-ва М.,
р-римость их в воде и соляной
к-те. О составе М. судят по характерным хим. р-циям и по цвету пламени газовой
горелки при внесении в него образца. Точная диагностика М. осуществляется в
лаб. условиях чаще всего оптическими (в поляризац. микроскопе) и рентгеновскими
(напр., на дифрактометре) методами. Элементный состав М. определяют методами
спектрального, атомно-абсорбц. анализа, лазерного спектрального микроанализа.
Электронно-зондо-вые методы позволяют определять состав микроколичеств М. и
устанавливать неоднородность и природу примесей без разрушения образца. Примеси
в М. изучают также с помощью электронной микроскопии и ЭПР. Электронное строение
М. исследуют методами ЭПР, ЯМР и мёссбауэ-ровской [мессбауэ-ровской] спектроскопии. Тип воды в
М. определяют методами термич. анализа, спектроскопии ИК и ЯМР. Явления структурной
упорядоченности и политипии М. изучают методами рентгенографии, электронографии,
спектроскопии ЯМР. Электронная микроскопия в сочетании с электронографией эффективны
при исследовании тонкодисперсных М.
Применение. М. служат
источниками для получения металлов и др. хим. элементов, а также хим. соединений.
Их используют как абразивные и огнеупорные материалы, применяют в керамике,
оптике, радиоэлектронике, электро- и радиотехнике. Нек-рые М. являются драгоценными
и поделочными камнями. Св-ва М. лежат в основе поиска и разведки полезных ископаемых,
методов сепарации и обогащения руд. В широких масштабах в пром-сти получают
синтетические М. для радиоэлектроники, оптики, абразивной и ювелирной пром-сти.
Лит.: Поваренных
А. С., Кристаллохимическая классификация минеральных видов, К., 1966; Булах
А. Г., Руководство и таблицы для расчета формул минералов, 2 изд., М., 1967;
Годовиков А. А., Введение в минералогию, Новосибирск, 1973; Марфунин А. С.,
Введение в физику минералов, М., 1974; Минералогические таблицы, Справочник,
под ред. Е.И.Семенова, М., 1981; Годовиков А. А., Минералогия, 2 изд., М., 1983.
Р. А. Виноградова.
|

