НИКЕЛЯ ГАЛОГЕНИДЫ
. Св-ва
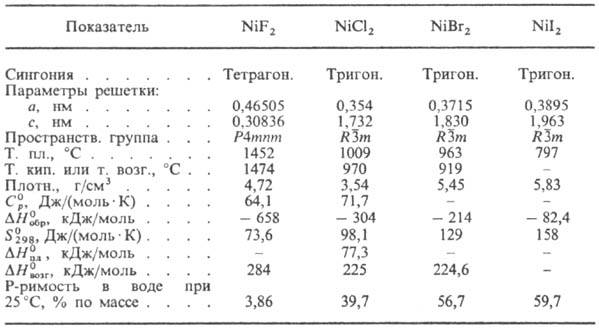
безводных дигалогенидов Ni приведены в табл. Д и ф т о р и д NiF2
образует зеленовато-желтые тетрагон. кристаллы типа рутила (ТiO2);
ур-ние температурной зависимости давления пара: lgp(мм рт.ст.) = 20,28-14650/T+
3,02 lg Т (298 -1220 К); устойчив на воздухе при комнатной т-ре, при
прокаливании окисляется до NiO; негигроскопичен; р-римость в воде почти не зависит
от т-ры; получают фторированием NiO, NiCl2 или др. соед. Ni. Из водных
р-ров NiF2 кристаллизуется в виде тетрагидрата NiF2•4Н2О
- светло-зеленые кристаллы; плотн. 2,219 г/см3; при ~ 120 °С
теряет одну молекулу воды, полностью обезвоживается в токе HF при 350-400 °С.
Безводный NlF2 используют как катализатор фторирования, для изготовления
катодов в хим. источниках тока, как компонент лазерных материалов.
Т р и ф т о р и д NiF3
образуется в виде розового осадка при электролизе расплава KHF2;
сильный окислитель; разлагается водой, выделяя из нее О2.
Известны производные т
е т р а ф т о р и д а NiF4, в частности K2[NiF6]:
розовые или темно-красные кристаллы кубич. сингонии; разлагается во влажном
воздухе; водой гидро-лизуется; получают фторированием смеси КСl с NiCl2;
используют как фторирующий реагент.
Д и х л о р и д NiCl2,
д и б р о м и д NiBr2 и дииодид NiI2 кристаллизуются в
ромбоэдрич. решетке типа CdCl2; для NlBr2 известна также
др. модификация со структурой типа CdI2; при прокаливании на воздухе
окисляются до NiO; безводные соли м. б. получены действием соответствующих галогенов
на Ni, обезвоживанием кристаллогидратов. Ди-хлорид - золотисто-желтые или желто-коричневые
кристаллы; ур-ние температурной зависимости давления пара: lgр(мм
рт.ст.) = 21,88-13300/T+ 2,68 lg T(298-1220 К); гигроскопичен;
раств. в воде, этаноле, гликоле. Из водных р-ров в интервале от — 53,4 до 28,8
°С кристаллизуется гексагидрат, при 28,8-64,3 °С-тетрагидрат, при 64,3-117,9°С-дигидрат.
Гексагидрат NiCl2.6H2O-кристаллы от светло-
до темно-зеленого цвета моноклинной сингонии (а = 1,023 нм, b =
= 0,705 нм, с = 0,657 нм, b = 122,16°, пространств. группа С2т);
плотн. 1,91 г/см3; в сухом воздухе выветривается, во влажном расплывается.
Тетрагидрат NiCl2.4H2O- кристаллы от желтовато-зеленого
до темно-зеленого цвета тетрагон. сингонии (а = 0,662 нм, с =
1,323 нм, пространств. группа P4mmm); плотн. 1,72 г/см3.
Дигидрат NiCl2.2H2O-бледно-желтые или коричневато-желтые
кристаллы моноклинной сингонии (а = 0,697 нм, b = 0,690 нм, с = 0,881 нм, b = 91,5°, пространств. группа I2/m); плотн.
2,56 г/см3; при ~ 140°С полностью обезвоживается. Применяют NiCl2
(и его гидраты) как компонент электролитов для рафинирования Ni и для никелирования,
для получения порошка Ni, как катализатор хлорирования орг. соед., безводный
NiCl2-как компонент термочувствит. красок.
СВОЙСТВА БЕЗВОДНЫХ ГАЛОГЕНИДОВ
НИКЕЛЯ
Из двойных хлоридов Ni
важнейший -NH4NiCl3.6H2O, получаемый
кристаллизацией из солянокислого раствора смеси NiCl2 с NH4Cl
при ~20°С; голубовато-зеленые кристаллы; раств. в воде; при 70 °С обезвоживается
(безводный NH4NiCl3-желтого или рубиново-красного цвета);
выше ~170°С разлагается; применяют как протраву при крашении, компонент
электролитов для никелирования.
Безводный NiBr2
- желто-коричневого цвета, безводный NiI2-стально-серый или черный;
гигроскопичны, раств. в воде, метаноле, этаноле, не раств. в диэтиловом эфире;
из водных р-ров кристаллизуются в виде гексагидратов. Гексагидрат NiBr2.6H2O-зеленые
кристаллы; при 28,5° теряет три молекулы воды, при ~ 200 °С полностью
обезвоживается. Описаны также ди- и нонагидраты NiBr2. Гексагидрат
NiI2.6H2O-голубовато-зеленые кристаллы; при
43 °С теряет две молекулы воды, при 140°С обезвоживается. Дибромид и
дииодид Ni используют для получения катализаторов, термочувствит. красок. П.
И. Федоров.
|

