НУКЛЕОЗИДНЫЕ АНТИБИОТИКИ
,
группа антибиотиков, имеющих строение нуклеозидов; их молекулы состоят из
моносахарида, связанного гликозидной связью с N- или С-атомами гетероцикла (агликона).
Н.а. способны участвовать в росте или функционировании разл. биол. систем, причем
небольшие изменения в структуре Н.а. часто ведут к принципиальному изменению
типа биол. действия.
Большинство Н.а.-структурные
аналоги прир. нуклеозидов и м.б. разделены на пуриновые и пиримидиновые антибиотики.
Далее можно выделить разл. группы с учетом структурных изменений в агликоне
или в углеводной части. Общепринятой классификации Н.а. нет.
Известны Н.а., близкие
по строению пуриновым и пири-мидиновым компонентам РНК, отличающиеся от них
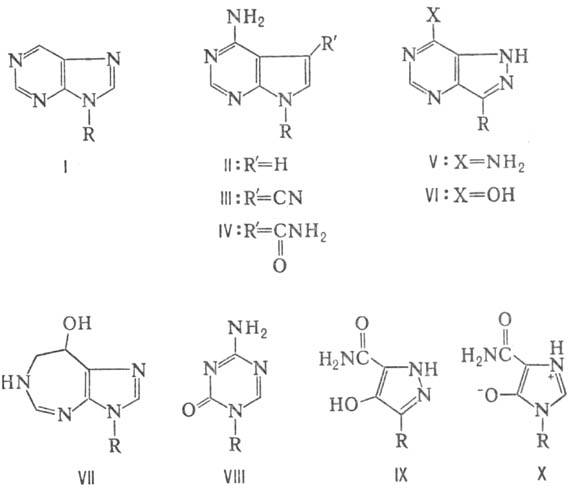
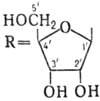
лишь заместителями в гетероцикле, напр. 9-b-D-рибофуранозил-пурин (небулярин;
ф-ла I). Многочисл. группу составляют Н.а., содержащие в молекуле гетероциклич.
основания, отличные от оснований в нуклеиновых к-тах. Примерами могут служить
N-нуклеозиды пирроло[2,3-d]-пиримидина-туберцидин (II), тойокамицин (III),
сангивамицин (IV), а также С-нуклео-зиды пиразоло[4,3-d]пиримидина -
форми-цин (V) и формицин В (VI). Эти в-ва включаются в нуклеиновые к-ты и(или)
нуклеотиды-коферменты, препятствуя их нормальному функционированию; очень токсичны;
нек-рые из них обладают высокой противовирусной или противоопухолевой активностью.
Коформицин (VII) и 2-дезоксикоформицин - аналоги переходного состояния дезаминирования
аденозина под действием аденозин-дезаминазы, ингибиторы этого фермента; используются
в клинике для потенцирования биол. эффекта нек-рых лек. препаратов, обладают
высокой противоопухолевой и имму-носупрессорной активностью.
Наиб. важный представитель
пиримидиновых Н.а., модифицированных по агликону,-притиволейкозный препарат
5-азацитидин (VIII). После фосфорилирования в клетке он включается в нуклеиновые
к-ты и ингибирует метилирова-ние последних. К Н.а. группы азолов относят, в
частности, пиразофурин (IX) и брединин (X). Первый из них ингибирует биосинтез
пиримидиновых нуклеотидов, обладает противоопухолевой активностью; второй-иммуносупрессор,
проявляет антиревматоидное действие.
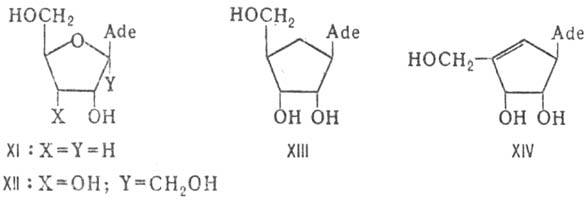
Пуриновые Н.а. с измененной
углеводной частью молекулы включают: аденинарабинозу (Ара-А; см. Противовирусные средства
); кордицепин (3-дезоксиаденозин, XI)-терминатор роста цепей РНК;
псикофуранин (XII)-ингибитор биосинтеза гуанозинмонофосфата. Высокой противоопухолевой
и противовирусной активностью обладают цикло-пентановые аналоги аденозина, сохранившие
конфигурацию его асимметрич. центров: аристеромицин (XIII)-ингибитор биол. метилирования,
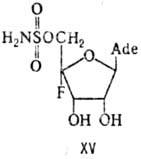
и неопланоцин (XIV)-ингибитор биосинтеза РНК. К аналогам аденозина относится
также нуклеоцидин (XV), к-рый связывает рибосомы и таким образом подавляет синтез
белка.
 XVI
XVI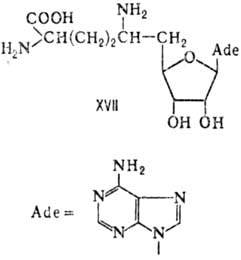
Примерами Н.а., содержащих
аминогруппу в кольце рибозы,
служат ингибиторы биосинтеза РНК 2-амино-2-дезоксигуанозин
и 3-амино-3-дезоксианозин. Др. тип биол.
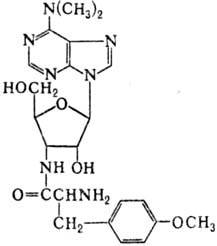
действия установлен у аминоациламинонуклеозидов, наиб.
важный представитель к-рых-пуромицин (XVI)-аналог аминоацил-тРНК, катализатор,
отщепляющий неполные пептидные
цепи от комплекса пептидил-тРНК-рибосома с образованием
пептидилпуромицина; терминатор пептидного синтеза.
Синефунгин (XVII)
и родственные ему Н.а.-ингибиторы метилтранс-феразы.
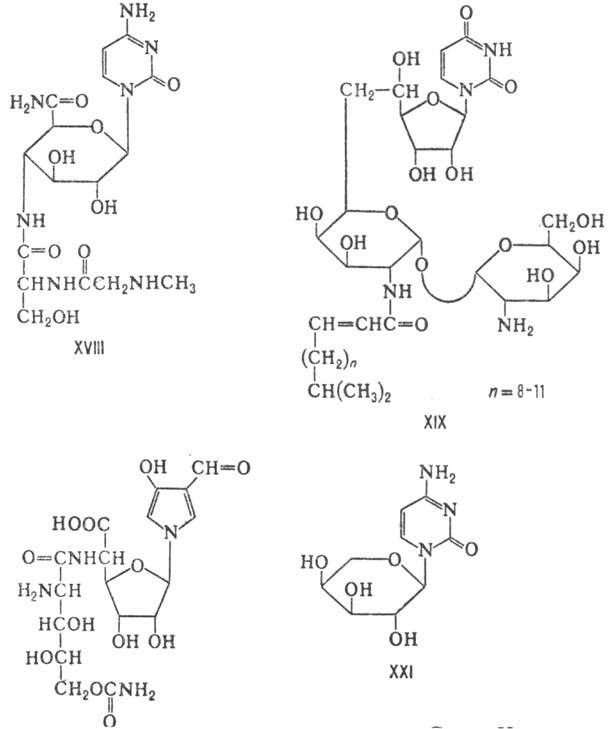
К пиримидиновым Н.а., модифицированным
по моно-сахариду, относят производные аминоациламиногексозил-цитозинов (напр.,
гугеротин, XVIII), к-рые ингибируют рибосомальную пептидилтрансферазу, что останавливает
пептидный синтез. Туникамицины (XIX)-структурные аналоги уридиндифосфатацетилглюкозамина-подавляют
процессы сборки, выделения и функционирования гликопро-теидов. У т.наз. полиоксинов
агликонами служат замещенный урацил или пиразол (как, напр., в случае полиоксина
N, XX), а углеводной частью - замещенная 5-амино-5-дезокси-аллофуранозуроновая
к-та. Эти соед.-сильные ингибиторы биосинтеза хитина. К Н.а. группы цитозина
относят пенто-пиранины, напр. пентопиранин Е (XXI).
XX
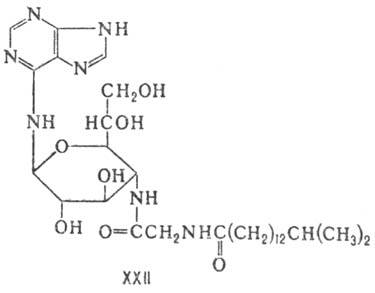
Среди Н.а. иног ,. да выделяют
группу нуклеозидов, мод и ф и ц и р о в а н н ы х одновременно и по агликону,
и по моносахариду. К ней можно отнести, в частности, септацидин (XXII), представляющий
собой N-6-з а м е щ
е н н ы й аденин.
Н.а. получают обычно микробиологич.
реже хим. синтезом
Применяют гл. обр. в мед.-биол.
исследованиях; лишь очень немногие
из них (напр., 5-азацитидин, Ара-А) используют в мед.
практике.
Лит.: Suhadolnik
R.J., Nucleoside antibiotics, N.V., 1970; его же, Nucleo-sides as biological
probes, N.Y., 1979. M. H. Преображенская.
|

