|
Реклама |
|
|
 |
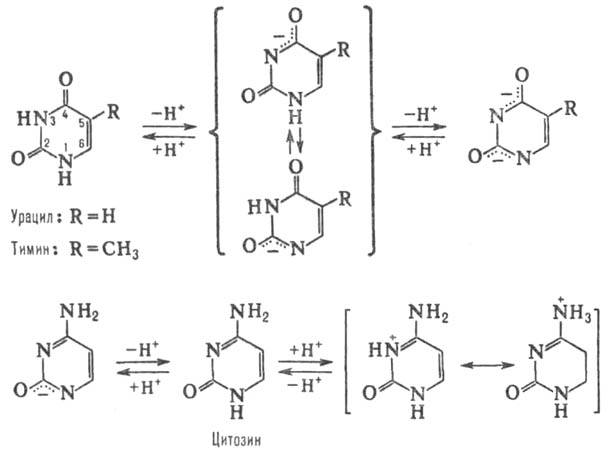
Наиб. характерные р-ции
П. о. с нуклеофилами - присоединение по связи C=C (гидросульфита, гидроксиламина,
галогена и др.) и замещение экзоциклич. аминогруппы цитозина (напр., р-ции с
гидроксиламинами, гидразинами). Последняя р-ция значительно облегчается при
насыщении связи C=C. Восстановление двойной связи C=C легко осуществляется путем
каталитич. гидрирования или действием NaBH4 при УФ облучении. Атом
H у С-5 легко замещается на гидрокси- или аминометильную группу, галоген. При
действии P2S5 один или оба атома О в урациле и тимине
могут замещаться на атом S. При действии на цитозин HNO2 происходит
его дезаминирование с образованием урацила. Р-ции П. о. с электроф.
реагентами (наиб. изучено алкилирование) идут преим. по атомам N-1 и N-3, в
меньшей степени - по экзоциклич. аминогруппе цитозина. В щелочной среде идет
также алкилирование по атомам О. Довольно легко протекает ацилирование аминогруппы
цитозина. При радиолизе водных р-ров
П. о. образуются 5,6-дигид-рокси-, 5-гидрокси-6-гидроперокси- и 5-гидроперокси-6-гидрокси-5,6-дигидропиримидины
и продукты их дальнейших превращений. Действие УФ излучения (l > 200
нм) на водные р-ры П. о. приводит к образованию 5,6-дигидро-6-гидроксипиримидинов
(фотогидратов), циклобутановых димеров (через триплетное состояние) с раскрытием
связей C=C, нециклобутановых димеров П. о. (через нижнее синглетное возбужденное
состояние). Фотогидраты спонтанно превращ. в исходные соед., а циклобутановые
димеры дедимеризуются фотохимически. Различие реакц. способности
П. о. позволяет избирательно модифицировать их в составе полинуклеотидов. Такие
р-ции лежат в основе определения нуклеотидной последовательности (первичной
структуры) нуклеиновых к-т. Взаимод. с соседними основаниями, зависящие от локальной
высшей структуры полинуклеотидов, оказывают влияние на скорость модификации
П. о. при действии разл. агентов. В связи с этим сопоставление относит. скоростей
модификации П. о. используется для изучения вторичной и третичной структуры
нуклеиновых к-т. Как канонические, так и
минорные П. о. обычно получают препаративно из нуклеиновых к-т путем кислотного
гидролиза и послед. разделения. Лит.: Кочетков H.
К. [и др.], Органическая химия нуклеиновых кислот, M., 1970; Бородавкин А. В.
[и др.], Электронная структура, УФ-спектры поглощения и реакционная способность
компонентов нуклеиновых кислот, в сб.: Итоги науки и техники, сер. Молекулярная
биология, т. 14, M., 1977; Шаба-ров а 3. А., Богданов А. А., Химия нуклеиновых
кислот и их компонентов, M., 1978; Photochemistry and photobiology of nucleic
acids, v. 1 (Chemistry), ed. by Shi Yi Wang. N. Y., 1976. Э.И. Будовский. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

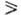 300
0C) бесцв. кристаллич. соед., умеренно раств. в горячей воде, не
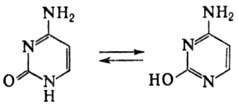
раств. в этаноле и диэтиловом эфире. Существуют в тауто-мерных формах (константы
таутомерного равновесия
300
0C) бесцв. кристаллич. соед., умеренно раств. в горячей воде, не
раств. в этаноле и диэтиловом эфире. Существуют в тауто-мерных формах (константы
таутомерного равновесия 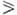 105),
напр.:
105),
напр.: