ПРИСОЕДИНЕНИЯ РЕАКЦИИ
,
происходят с объединением двух молекул в одну. Наиб. распространены П. р.
с участием субстратов, имеющих кратные связи; при этом происходит разрыв одной
p-связи и образование одной или двух s-связей. Для обозначения П.
р. используют символ Ad (от англ. addition - присоединение); для р-ций
циклоприсо-единения такой символ не применяют.
В зависимости от природы
субстрата различают П. р. по изолированным или сопряженным кратным связям, напр.:
С=С, С=С, С=С—С=С, С=О, C=N, С=N. Различают р-ции гомолитич. (AdR)и гетеролитич. присоединения. Последние в зависимости от заряда атакующего
реагента подразделяют на р-ции электроф. (AdE)и нуклеоф.
(AdN)присоединения. Поведение реагента зависит от типа субстрата
и условий проведения р-ции (р-ритель, присутствие катализатора, действие УФ
облучения и др.). Мн. реагенты в разных условиях могут проявлять разл. виды
реакц. способности, напр. галогены могут выступать в роли радикальных, электроф.
и даже нуклеоф. агентов.
Наиб. изучены П. р. по
кратным связям углерод-углерод. Эти процессы протекают по ступенчатому (стадийному)
или синхронному (согласованному) механизму. При ступенчатом механизме первая
стадия-атака нуклео-фила, электрофила или своб. радикала, вторая - рекомбинация
получающегося интермедиата с положит., отрицат. или нейтральной частицей, напр.:
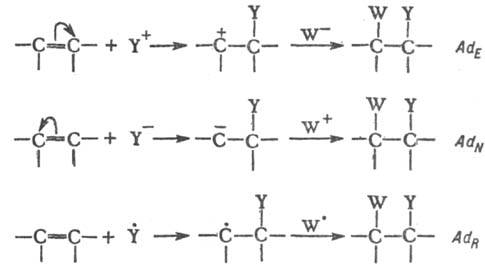
Электроф. или нуклеоф.
частицы не обязательно должны быть ионами; они могут представлять собой электроноак-цепторную
или электронодонорную часть (группу) молекулы. Р-ции AdN возможны
лишь со связями С=С, активированными электроноакцепторными заместителями;
для реализации AdE нужны либо незамещенные связи С=С, либо
активированные электронодонорными заместителями. Для р-ции AdR
характер заместителя при связи С=С большого значения не имеет.
Стереохим. результат ступенчатого
присоединения зависит от механизма р-ции и природы реагирующих соединений. Так,
электроф. присоединение к олефинам может протекать как сын-присоединение- частицы
Y и W атакуют молекулу с одной стороны плоскости двойной связи либо как анти
-присоединение
- частицы атакуют с разных сторон плоскости; в нек-рых случаях р-ции идут нестереоспецифич-но.
Нуклеоф. присоединение с участием карбанионов протекает, как правило, нестереоспецифично.
При П. р. по тройным связям син
-присоединение приводит к цис
-изомеру,
анти
-присоединение - к транс
-изомеру.
В случае синхронного механизма
атака на оба атома С осуществляется одновременно и р-ция протекает как диполярное
присоединение (см. Циклоприсоедшение), при этом П. р. по двойной
или тройной связи идут как сын-присоединение (см., напр., Реппе реакции
).
П. р. по сопряженным двойным
связям, протекающие по ступенчатому механизму, приводят к образованию продуктов
1,2- и 1,4-присоединения:
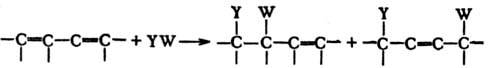
Синхронное 1,4-присоединение
к диенам протекает след. образом:
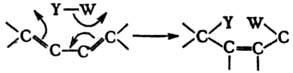
Особый вид П. р.-сопряженное
присоединение. Протекание таких р-ций сопровождается связыванием р-рителя (или
специально добавленного реагента) на завершающей стадии процесса. Напр., сопряженное
электроф. присоединение галогенов к алкенам в СН3СООН приводит наряду
с 1,2-дига-логенидами к b-ацетоксиалкилгалогенидам:
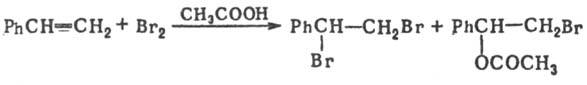
Примеры сопряженного нуклеоф.
присоединения - Михаэля реакция
и взаимод. активированных алкенов с цианид-анионом
в протонных р-рителях SH:
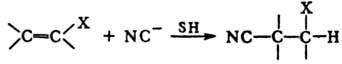
В случае П. р. по кратным
связям углерод-гетеро-атом, в к-рых положит. заряд локализован на атоме С (связи
С=О, C=N, С = N и C=S), нуклеофилы всегда присоединяются к атому С, а
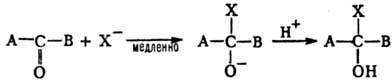
электрофилы-к гетероатому. В наиб. степени изучены нуклеофильные П. р. по карбонильной
группе:
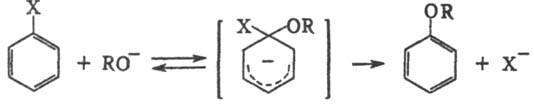
П. р. по атому С может
быть одной из стадий р-ции замещения в ароматич. ряду, напр.:
К П. р. относят образование
ониевых солей, а также многочисленные и разнообразные внедрения реакции
,
напр.:
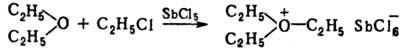

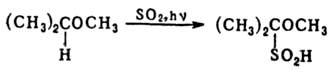
П. р., в к-рых происходит
многократное присоединение одной и той же молекулы (мономера) к активной частице,
наз. ргциями олигомеризации или полимеризации (см. Полимеризация
). См. также Рекомбинация
, Протонирование
.
Лит.: Органикум,
т. 1, М., 1979, с. 325; Общая органическая химия, пер. с англ., т. 1, М., 1981,
с. 198; то же, т. 2, М., 1982, с. 507; Марч Дж., Органическая химия, пер. с
англ., т. 3, М., 1987, с. 132-440; Hegarty A. E., Rigopoulos P., RoweJ.E., "Austral.
J. Chem.", 1987, v. 40, №10. p. 1777-82. А. А. Соловьянов.
|

