ПРОТОНИРОВАНИЕ
, процесс
переноса протона с к-ты на прогофильную частицу (основание):
АН + В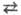 А-
+ ВН+ АН-к-та, В-основание
А-
+ ВН+ АН-к-та, В-основание
Доноры протонов в П.-к-ты
Брёнстеда [Бренстеда] (см. Кислоты и основания
), в частности ОН-, NH-, СН- и вообще
ЭН-кис-лоты (см. СН-кислоты
), акцепторы-разл. основания. Возможность
протекания П. обусловлена относит. силой к-ты и основания. Напр., для таких
сильных оснований, как карбанионы или амидные анионы, донорами протонов могут
служить весьма слабые СН-кислоты; сильные протонные к-ты и особенно сверхкислоты
(см. Кислоты неорганические
) позволяют осуществить протонирование
таких молекул, как карбоновые к-ты и даже насыщ. углеводороды, напр.:
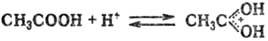
П. может происходить как
межмолекулярно, так и внут-римолекулярно и сопровождаться перемещением кратной
связи, образованием циклич. структуры, изменением валентности атома, к к-рому
мигрирует протон, и др. превращениями.
П. протекает с очень высокой
скоростью. Так, в водных р-рах протонирование оснований типа анионов неорг.
и орг. к-т, алкоксид-ионов, феноксид-ионов, аминов, циклич. N-oc-нований происходит
обычно с константой скорости k ок. 1010 дм3/(моль·с).
Быстрее всего протонируется НО- [ок. 1,5·1011 дм3/(моль·с)],
что обусловлено перемещением Н+ по эстафетному механизму, по депочке
водородных связей. В случае П. карбанионов k варьирует в очень широких
пределах [~ от 1 до 1010 дм3/(моль·с)] из-за необходимости
перестройки электронной или геом. структуры протофиль-ной частицы при переносе
протона. На скорость П. в неводных средах сильное влияние оказывают сольватация
и ионная ассоциация.
Количеств. данные о кинетике
и механизме П. получают с помощью спец. методов изучения быстрых р-ций (см. Струевые кинетические методы
, Релаксационные методы
, Электрохимическая кинетика
).
Информацию о тонких деталях
механизма П. дают зависимости (соотношения Брён-стеда [Брен-стеда]) k от кислотности
(рКа) или основности (рКb) участвующих
в П. реагентов и величины кинетич. (первичного и вторичного) изотопных эффектов
и изотопного эффекта р-рителя. Предполагается, что в нек-рых хим. процессах
П. может происходить без преодоления энергетич. барьера (туннельный эффект).
Енолизация, изотопный водородный
обмен, ионный обмен, гидролиз, гидратация, этерификация-явления, в к-рых П.-обязательная
или возможная стадия.
Лит.: Шатенштейн
А. И., Теории кислот и оснований, М.-Л., 1949; Меландер Л., Изотопные эффекты
в скоростях реакций, пер. с англ., М., 1964; Белл Р., Протон в химии, пер. с
англ., М., 1977; Гордон Дж., Органическая химия растворов электролитов, пер.
с англ., М., 1979; Химия гиперкоординиро-ванного углерода, пер. с англ., М.,
1990, с. 169-229, 253-327.
А. А. Соловьянов.
|

