ПШОРРА СИНТЕЗ
, получение
производных фенантрена конденсацией ароматич. о-нитроальдегидов с арилуксусны-ми
к-тами и послед. превращениями продуктов конденсации, напр.:
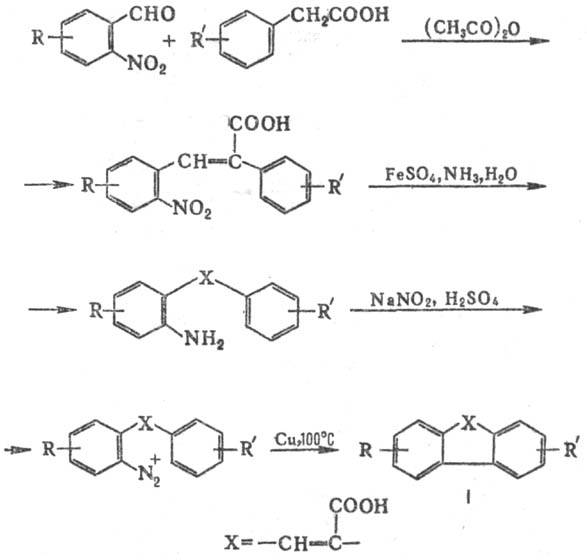
Последняя стадия (циклизация
диазосоединения) имеет самостоят. значение (т. наз. р-ция Пшорра) и применяется
для синтеза не только производных фенантрена, но и разнообразных полициклич.
соед. (ф-ла I; Х = СН2, СН2СН2, С=O, О, S,
Se, NR, CONH, OCH2, CH2Se).
В зависимости от условий
р-ция протекает по разным механизмам. При катализируемом медью разложении диазосоединения
в кислой или щелочной среде происходит гл. обр. образование ассоциированных
с пов-стью катализатора арильных радикалов и их циклизация; наряду с этим происходит
циклизация образовавшихся арильных катионов:
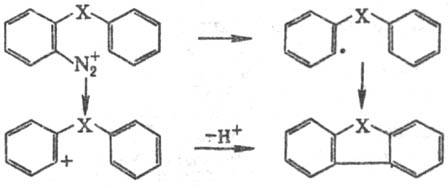
При термич. разложении
диазосоединений без катализатора преобладающим становится образование катионов
и их циклизация, а гомолитич. процессы играют меньшую роль.
Оптим. условия проведения
р-ции Пшорра определяются строением исходных соединений. Если ароматич. кольцо,
не содержащее диазогруппу, дезактивировано к электроф. атаке, макс. выход достигается
в условиях, благоприятствующих гомолитич. процессу, напр.:
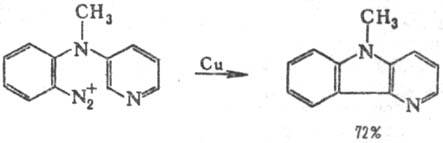
Методы проведения р-ции
по гомолитич. механизму включают обычно стадию диазотирования алкилнитритами
в неводной среде и восстановление диазосоединений до радикалов с помощью KI,
КВг, NaHSO3, NaH2PO3, Ti2(SO4)3
или пиридина, а также электрохимически либо фотолитически.
Циклизация по гетеролитич.
механизму осуществляется в условиях, при к-рых эффективно генерируется арильный
катион (отсутствие внеш. нуклеофилов и промоторов образования радикалов), напр.:
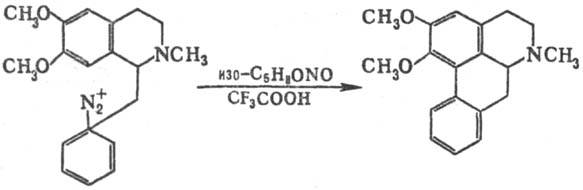
Если заместители в цикле,
не содержащем диазогруппу, расположены асимметрично, то замыкание кольца может
осуществляться с участием разл. положений этого цикла.
Высокая реакц. способность
диазогруппы обусловливает ряд побочных р-ций-ее замещение водородом, гидрокси-лом,
галогеном, межмол. арилирование и др.
П. с. используют в лаб.
практике для получения производных фенантрена; р-цию Пшорра применяют в синтезе
разл. гетероциклов, особенно алкалоидов.
Циклизация диазосоединений
открыта в 1894 рядом исследователей; Р. Пшорр в 1896 применил ее для получения
фенантрен-9-карбоновой к-ты и в дальнейшем подробно изучил эту р-цию, а также
синтез фенантренов исходя из ароматич. о-нитроальдегидов.
Лит.: Де Тар Д.
Л. Ф., в сб.: Органические реакции, пер. с англ., сб. 9, М., 1959, с. 529-600;
Общая органическая химия, пер. с англ., т. 1, М., 1981, с. 423-25; Abramovitch
R., в кн.: Advances in free-radical chemie, v. 2, N. Y., 1967, p. 87-138; Sieper
H.,"Chem. Ber.", 1967, Bd 100, № 5, S. 1646-54; Kametani Т., Fukumoto
K., "J. Heterocycl. Chem.", 1971, v. 8, p. 341-56; Hegarty А., в
кн.: The Chemistry of diazonium and diazogroups, ed. by S. Patai, N.Y., 1978,
pt 2, p. 511-91; Duclos R., Tung S., Rapoport H., "J. Org. Chem.",
1984, v. 49, № 26, p. 5243-46. Д. В. Иоффе.
|

