РАДЗИШЕВСКОГО РЕАКЦИЯ
,
получение амидов кар-боновых к-т взаимод. нитрилов с Н2О2
в щелочной среде:
RCN + 2Н2O2
: RC(O)NH2 + О2 + Н2О
Р-ция экзотермична. Ее
обычно проводят в водном этаноле или метаноле при 40-70 °С, концентрации
Н2О2 3-6%, щелочи 1-20%. Малореакционноспособные нитрилы,
напр, о-толунитрил, превращают в амиды действием 10-30% Н2О2.
Электроноакцепторные заместители в R ускоряют р-цию. Выходы ароматич. амидов
80-90%, алифатических 40-60%.
Механизм Р. р. предполагает
нуклеоф. атаку нитрила гидропероксид-анионом с образованием неустойчивого ин-термедиата
(I), к-рый является окислителем; далее следует гидридный перенос от второй молекулы
Н2О2 к этому интермедиату:
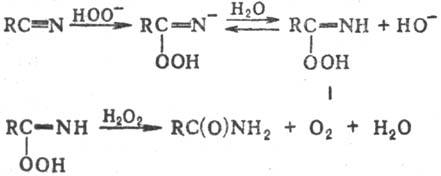
Часто р-ция сопровождается
хемилюминесценцией вследствие перехода образующегося О2 из синглетного
в триплет-ное состояние.
Одновременно с образованием
амидной группы в нек-рых случаях возможно окисление функц. групп субстрата,
напр. из ненасыщ. нитрилов образуются эпоксиамиды, а из пири-динкарбонитрилов
- N-оксиды амидов:
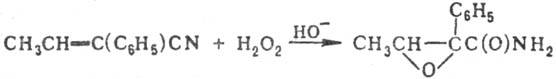
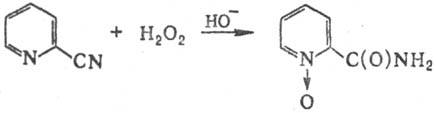
Нек-рые a,b-ненасыщ.
нитрилы образуют не эпоксиамиды, а ненасыщ. амиды или эпоксинитрилы, напр.:
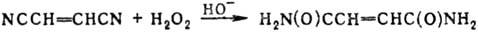
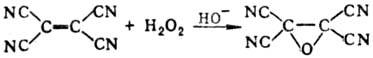
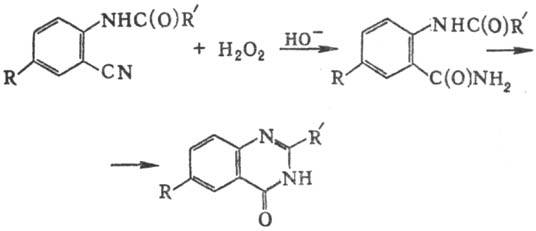
С помощью Р. р. из N-ацилантранилонитрилов
можно получить замещенные хиназолоны:
Разновидность Р. р.-действие
Н2О2 на смесь нитрила (напр., бензонитрила) с легкоокисляющимся
в-вом. В этом случае наряду с амидом образуются с высоким выходом продукты окисления
др. в-ва, напр. из циклогексена - цикло-гексеноксид (выход 85%), из пиридина-пиридин-1-оксид
(79%), из анилина - азобензол (62%).
Р. р. используют для получения
амидов карбоновых к-т и эпоксисоединений. Она открыта в 1885 Б. Радзишевским.
Лит.. Физер Л.,
Физер М., Реагенты для органического синтеза, пер. с англ., в. 3, М., 1970,
с. 74-76; Зильберман Е. Н., Реакции нитрилов, М., 1972, с. 74-78. С. К. Смирнов.
|

