АЛЬДИМИНЫ И КЕТИМИНЫ
, производные альдегидов и
кетонов, в к-рых атом кислорода карбонильной группы замещен иминогруппой
=NH. Общая ф-ла альдиминов-RCH=NH, кетиминов-RRC=NH.
Назв. А. и к. производят от назв. двухвалентного радикала RRC= прибавлением
слова "амин" или от названия соед. RRCH2 присоединением суффикса
"имин" (либо префикса "имино"), напр. СН3СН=NН-этилиденамин
или этанимин. Применяются также традиц. назв., образованные от назв. альдегидов
или кетонов, напр. СН3СН=NH-ацетальдимин, (С6Н5)2С=NН-дифенилкетимин,
или бензофенонимин.
А. и к.-жидкие или твердые в-ва; не раств. в воде, раств. в орг. р-рителях.
Производные альдегидов и низших алифатич. кетонов неустойчивы, легко тримеризуются,
напр.:
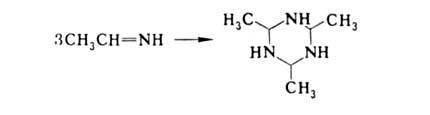
Длина связи C=N 0,129-0,131 нм, энергия 6 кДж/моль; расчетное значение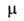 3,0*10-30 Кл-м. ИК-спектр: VNH 3400-3300 см-1,
vC=N 1650-1640, 1635-1620 и 1603 см-1 соотв.
для алифатич., жирноароматич. и ароматич. кетиминов.
3,0*10-30 Кл-м. ИК-спектр: VNH 3400-3300 см-1,
vC=N 1650-1640, 1635-1620 и 1603 см-1 соотв.
для алифатич., жирноароматич. и ароматич. кетиминов.
А. и к. - слабые основания (напр., для дифенилкетимина рКа7,18);
образуют с к-тами в безводной среде иминиевые соли, напр. (С6Н5)2С=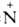 Н2Сl.
При взаимод. с алкилга-логенидами превращаются в N-замещенные А. и к. -
основания Шиффа RRC=NR", при ацилировании-в N-ацилпроизводные RRC=NCOR",
при р-ции с гипохлоритами - в неустойчивые N-хлорпроизводные, перегруппировывающиеся
в
Н2Сl.
При взаимод. с алкилга-логенидами превращаются в N-замещенные А. и к. -
основания Шиффа RRC=NR", при ацилировании-в N-ацилпроизводные RRC=NCOR",
при р-ции с гипохлоритами - в неустойчивые N-хлорпроизводные, перегруппировывающиеся
в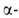 аминокетоны:
аминокетоны:
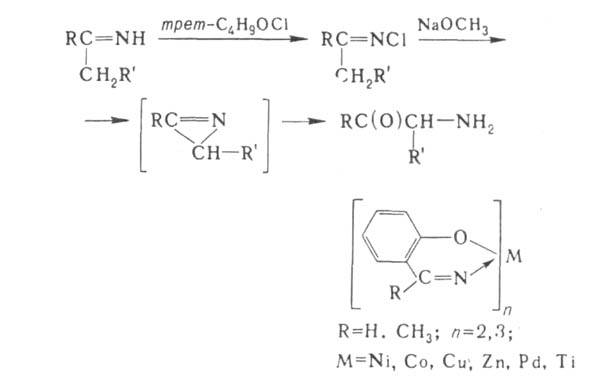
С солями металлов А. и к. образуют внутрикомплексные соединения [особенно
прочные, если в исходных молекулах содержится протонодонорная группа в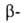 (или орто)-положе-нии к группе C=N], например:
(или орто)-положе-нии к группе C=N], например:
Нуклеофилы присоединяются к А. и к. (особенно легко к соответствующим
иминиевым солям) по связи С—N. Схема нек-рых превращений А. и к. приведена
ниже:
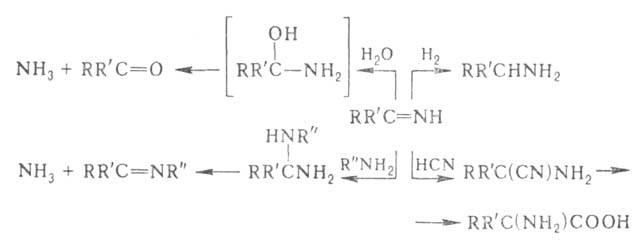
Р-цию с HCN используют для лаб. и пром. получения аминокислот (см. также Штреккера реакции
).
Альдимины синтезируют восстановлением нитрилов: действием SnCl2
в присут. НС1 в среде эфира (р-ция Стефена); комплексными гидридами металлов
NaAlH4, NaBH4, NaAl(C2H5O)3H;
водородом на катализаторах. Последнюю реакцию удается остановить на стадии
образования альдиминов, если возникает комплекс альдимина с катализатором
(как, например, при получении салицилальдимина).
Кетимины синтезируют присоединением к нитрилам металлоорг. соед. (Mg,
Li, Zn, A1), напр.:
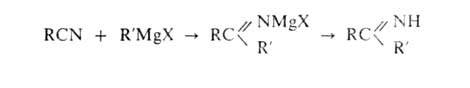
А. и к. получают также взаимод. фенолов и их эфиров с HCN или нитрилами
(кат.-хлориды Zn, Cu, Fe):
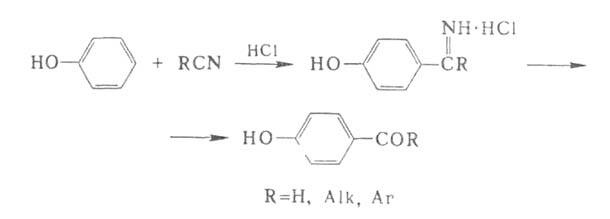
Гидролизом образовавшихся продуктов в пром-сти получают альдегиды и
кетоны (см. также Гаттермана синтез
, Хеша реакция).
Ароматические кетимины получают: пропусканием NH3 через расплав
кетона или взаимодействием NH3 и кетона в присутствии ThO2;
р-цией кетонов с фосфинимидами (Штаудингера р-ция):
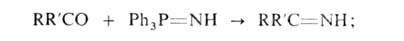
взаимод. NH3 с дигалогенпроизводными кетонов, напр. с дифенилдихлорметаном
(С6Н5)2СС12.
А. и к. определяют: титрованием хлорной к-той в неводных средах (хлороформ,
диоксан, ацетонитрил); по кол-ву карбонильных соед., образующихся при гидролизе;
полярографически.
А. и к.-промежут. продукты нек-рых р-ций (напр., Лей-карта, Соммле).
Ароматич. А. и к., содержащие в орто-
положении гидроксигруппу (напр.,
салицилальдимин, о-гидроксиацетофенонимин),-хелатообразующие агенты.
Комплексы этих А. и к. с Си или Со-катализаторы окисления фенолов кислородом
до хинонов, комплексы с Ti или W-сокатализаторы полимеризации непредельных
соед. на алюминийорг. соединениях.
Лит.. Зильберман Е.Н., Реакции нитрилов, М., 1972; Общая органическая
химия, пер. с англ., т. 3, М., 1982, с. 476-646. Д.В. Иоффе.

