СУБЛИМАЦИЯ
(возгонка,
от лат. sublimo- возношу), переход в-ва из твердого состояния непосредственно
(без плавления) в газообразное. С. подчиняется общим законам испарения
. Обратный
процесс -конденсация
в-ва из газообразного состояния, минуя жидкое, непосредственно
в твердое состояние-наз. десублимацией (Д.). С. и Д.-фазовые переходы первого
рода.
Сублимац.-десублимац. процессы
(СД процессы) могут протекать без участия и с участием т. наз. р-рителей-инертных
(не претерпевающих фазовых переходов) газообразных или твердых компонентов.
СД процессы с р-рителями проводят при атм. или повыш. давлении, без р-рителей-в
вакууме.
В СД процессах с р-рителями
инертное газообразное в-во (газ-носитель) служит для переноса паров сублимируемых
(десублимируемых) в-в, а также для охлаждения газовых смесей при Д. Инертное
твердое в-во вводят в систему: в качестве носителя для переноса продукта Д.-десублимата
(напр., при фракционной сублимац. очистке в-в, см. ниже); для интенсификации
подвода теплоты; для обеспечения равномерного индукционного или высокочастотного
нагрева исходного материала и т.д.
Д. осуществляется на твердые
пов-сти или происходит в объеме газовой фазы с выделением твердого в-ва в виде
частиц аэрозоля.
Известны природные СД процессы,
напр.: образование газовых гидратов
, образование и изменение ядер комет,
Д. водяного пара в атмосфере, С. льда.
Механизмы. С.-эндотермический,
а Д.-экзотермический процессы. В случае С. при подводе энергии (конвективный
или контактный нагрев,
нагрев излучением, напр. лазерным) происходит разрыв межмол. связей. Сублимир.
в-ва м. б. конечными продуктами или направляться на Д., перед к-рой могут подвергаться
промежуточной обработке, напр. ад-сорбц. очистке.
При Д. (процесс самоорганизации
)возникают ван-дер-ваальсовы связи между отдельными молекулами в-ва с выделением
энергии, к-рую отводят от десублимата не-посредств. контактом его с охлаждаемой
твердой пов-стью, взаимод. с вводимым дополнительно хладагентом, испарением
жидкости (напр., воды), добавляемой в газовую смесь, ее расширением.
Газовая фаза чаще всего
образует идеальную смесь компонентов. Твердая фаза может образовывать системы,
в к-рых компоненты полностью взаимно нерастворимы, неограниченно взаимно р-римы,
ограниченно р-римы. Характер твердых систем определяет в осн. инженерное оформление
СД процессов.
Статика. СД процессы,
как и др. процессы с фазовыми переходами первого рода, удобно представлять с
помощью трехфазной диаграммы состояния
(рис. 1). На этой диаграмме сублимац.
процесс изображен пунктирными линиями, пересекающими кривую с в точке
ниже тройной точки Тр при повышении т-ры и постоянном давлении либо при понижении
давления и постоянной т-ре.
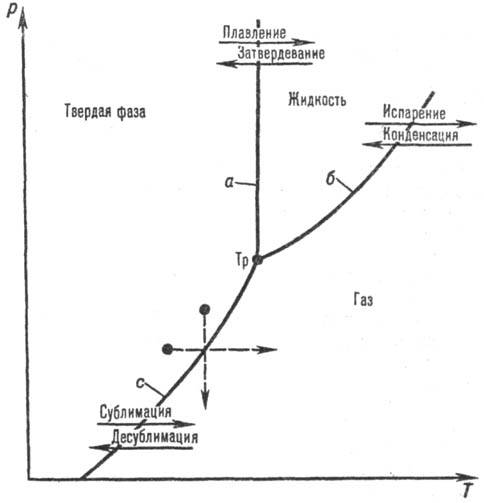
Рис. 1. Фазовая диаграмма
для сублимац.-десублимац. процессов: а. Ъ. с-кривые давления пара соотв.
при плавлении в-ва, над жидкостью, над твердой фазой, Тр-тройная точка; p-давление;
T-абс. т-ра.
В случае однокомпонентных
систем ур-нием кривой с служит Клапейрона -Клаузиуса уравнение
для
давления на-сыщ. пара над твердой фазой при энтальпии С. DHС
= const и абс. т-ре Т:
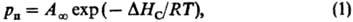
где A,-константа,
R-газовая постоянная.
Для многокомпонентных систем
ур-ние для рп по форме аналогично ур-нию (1), но зависит
от характера взаимод. компонентов.
При Д. переход от гомогенной
системы к гетерогенной начинается с образования единичных элементов новой фазы-твердых
зародышей (кластеров), к-рые после достижения критич. размера имеют тенденцию
к неограниченному росту. Энергия кластеров увеличивается с возрастанием числа
входящих в них молекул, стремясь асимптотически к пределу, равному теплоте фазового
перехода. Термодинамически возможность протекания СД процессов определяется
соотношением:
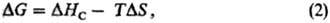
где энергия Гиббса DG
< 0; DS-
изменение энтропии системы. При равновесии DG
= 0. С повышением т-ры увеличивается термодинамич. вероятность протекания С.
Изменение DНС для молекул, содержащих более 5
атомов, составляет 4-8 кДж/моль. Для молекул с мол. массой М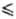 100
изменение энтропии DS = 120-140, для М > 100-от 140
до 160кДж/(моль·К).
100
изменение энтропии DS = 120-140, для М > 100-от 140
до 160кДж/(моль·К).
Кинетика. С. - многостадийный
процесс, для проведения к-рого необходима дополнит. тепловая энергия. При ее
подводе частицы в-ва мигрируют на пов-сти твердой фазы из состояния с наиб.
прочностью связей в состояние с их меньшей прочностью, а затем в газовую фазу.
Одновременно из нее происходит Д. частиц. При равновесии число десублимировавшихся
на пов-сти частиц отличается от числа частиц, ударяющихся о пов-сть. Соотношение
указанных потоков определяется т. наз. коэффициентом конденсации или С. a
(О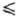 a
a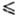 1).
Макс. скорость СД процессов наиб. просто находят при их проведении в вакууме
по ур-нию Герца-Кнудсена;
1).
Макс. скорость СД процессов наиб. просто находят при их проведении в вакууме
по ур-нию Герца-Кнудсена;
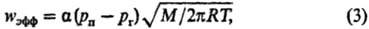
где рг-давление
паров в-ва в газовой фазе.
Скорости С. и Д. обусловливаются
прежде всего скоростью разрушения кристаллов при С. и скоростью кристаллизации
при Д., а также скоростями переноса массы от пов-сти твердой фазы в газовый
поток. По мере протекания С. и Д. изменяются характеристики твердой фазы (толщина
и пористость слоя, шероховатость пов-сти и др.) и соотв. интенсивность тепло-
и массообмена с газовой фазой.
Аппаратурное оформление
и технологические схемы СД процессов. При их осуществлении необходимо обеспечить
ввод в систему твердой фазы и подвод к ней энергии, перемещение пара в газовой
фазе, выполнение осн. цели (напр., разделения компонентов), отвод тепловой энергии
при Д.; выделение продукта на твердой пов-сти или в объеме газовой фазы, отделение
газа-носителя от оставшегося в виде пара или аэрозоля продукта; поддержание
в системе необходимых давления и т-ры.
Оборудование для проведения
СД процессов включает системы нагрева и охлаждения, подачи газовых потоков,
вакуумные, транспортирования твердой фазы и управления процессом. Аппараты для
собственно С. и Д. чрезвычайно разнообразны: трубчатые (без оребрения и с разл.
оребре-нием), полочные (в т.ч. с вращающимися полками), роторные вихревые, колонные
с псевдоожиженным слоем, вакуумные камеры и т.д. Основа расчета таких аппаратов-мат.
модели, включающие ур-ния переноса массы, теплоты и импульса в рабочем объеме
для паровой фазы и частиц аэрозоля, кинетич. зависимости для разрушения и роста
твердой фазы, описание изменения пористой структуры этой фазы и ее поверхностной
шероховатости.
Один из важных параметров
СД процессов-кол-во подводимой (отводимой) теплоты. Для С. данный параметр определяется
теплотой фазового перехода, в случае Д. предварительно находят необходимую величину
охлаждения газа по ур-нию:
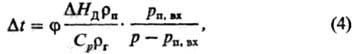
где f-степень улавливания
в-ва; DHД- энтальпия Д.; rп, rг-плотность
пара в-ва и газа-носителя; Ср-теплоемкость газа-носителя;
pп.вх-давление пара в-ва на входе в систему, p -общее
давление в ней.
В зависимости от назначения
СД процессов используют разные технол. схемы их проведения. Типичные примеры-схемы
очистки разл. в-в. Очистка включает простую (однократные С. и Д.) и фракционную
С. (многоступенчатая прямо- и противоточная, а также зонная; см. Кристаллизационные методы разделения смесей
): Простая С. может быть
вакуумной (рис. 2, а)или с газом-носителем, к-рый удаляется из системы
(рис. 2, б)либо рециркулирует в ней (рис. 2, в). При фракционной
С. может осуществляться рециркуляция как газообразного, так и твердого носителей
(рис. 2, г), что обеспечивает противоток фаз в сублимац. колонне. В этой схеме
инертные твердые нелетучие частицы подаются в десублиматор-дефлегматор над сублимац.
колонной при т-ре ниже точки Д. пара; здесь частицы покрываются тонкой пленкой
твердого десублимата, создающего обратный поток для укрепляющей части сублимац.
колонны. Более летучие компоненты концентрируются в ее верх. части, менее летучие-в
нижней. Противоток паровой фазы осуществляется под воздействием температурного
градиента (с возрастанием т-ры сверху вниз) либо введением в ниж. часть колонны
рециркулирующего инертного газа-носителя, создающего поднимающийся вверх поток
пара.
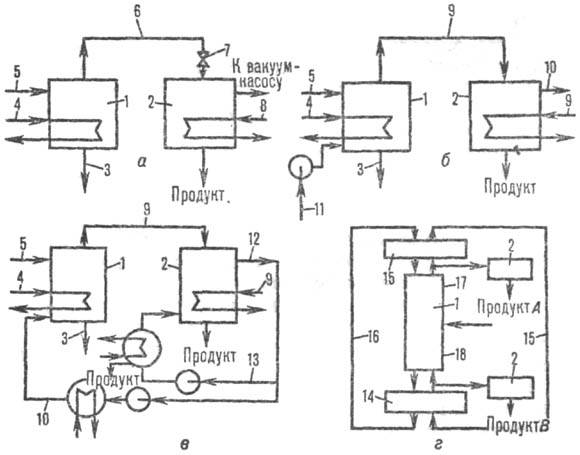
Рис. 2. Схемы сублимац.
очистки в-в: а-простая вакуумная сублимация; б-сублимация с инертным
газом-носителем; в-сублимация с рециклом газа-носителя; г-фракционная
сублимация с рециклами газа-носителя и твердого носителя; 1-сублиматор; 2-десублиматор-дефлегматор;
3-остаток в-ва; 4-нагреват. контур; 5-питание; 6-пар; 7-вентиль (для сублимации
из расплава -квазисублимации); 8-охлаждающий контур; 9-смесь пара и газа-носителя;
10, 11, 13-нагретый газ-носитель и его рецикл; 12-смесь газа-носителя и непро-цесублимир.
продукта; 14-испаритель; 15-десублиматор обратного потока· 16-рецикл твердого
носителя; 17, 18-укрепляющая и исчерпывающая секции.
Применение СД процессов.
К достоинствам этих процессов можно отнести: сравнительно высокий равновесный
коэф. разделения; возможность в случае использования газовых смесей исключить
испарение р-рителей (в отличие от абсорбции и ректификации); меньшая рабочая
т-ра (чем при дистилляции); удобство управления процессом нанесения покрытий;
возможность получать целевые продукты сразу в товарной форме (дисперсные частицы,
монокристаллы, твердые пленки), высокочистые материалы, композиции несплавляемых
компонентов (нитевидные кристаллы из неметаллов в металлич. матрице), тонкие
и сверхтонкие порошки металлов, их оксидов. Благодаря этим и др. достоинствам
СД процессы нашли широкое распространение (особенно начиная с 70-х гг.) в разл.
областях науки и техники.
Сублимац. очистке подвергают
неорг. (HfCl4, A1C13,I2, ряд металлов) и орг.
(антрахинон, бензойная и салициловая к-ты, цианурхлорид, фталоцианины) в-ва,
материалы для микроэлектроники. В криогенной технике СД процессы применяют для
очистки газовых смесей (см. Воздуха разделение
). К сублимац. очистке
относят также разделение изотопов урана.
СД процессы применяют для
выделения целевых продуктов из паровоздушных смесей (напр., фталевый и ма-леиновый
ангидриды), получения новых в-в (техн. углерод, алмазы в виде монокристаллов
или пленок и т.д.).
Сублимац. сушку (сушку
вымораживанием) используют в произ-вах капрона, лавсана и полиэтилена; для очистки
Sb2O3, CaF2, ZnS, камфоры, пирогаллола, салициловой
к-ты и др.; при получении антибиотиков, пищ. продуктов, мед. препаратов (плазма
крови, кровезаменители и т.п.).
СД процессы используют
для послойного анализа хим. состава твердых систем (с использованием метода
лазерного испарения); для нанесения защитных покрытий на микросферы ядерного
топлива, на пов-сти разл. в-в при изготовлении чувствит. датчиков (сенсоров)
состава и св-в газов, на пов-сти углеродных волокон и изделий из них, а также
на металлич. пов-сти (напр., хромирование); в технологии полупроводников и сверхпроводников;
при изготовлении светоизлучающих диодов, оптич. световодов и др. в опгоэлектронике;
для записи информации на лазерных оптич. дисках; при создании интегральных схем
в микроэлектронике; при тепловой защите сверхзвуковых аппаратов (см. Абляционные материалы
); при создании газодинамич. потоков (процессы, протекающие
при горении смесевых твердых ракетных топлив, и др.); для термопереводного печатания
(т.е. получения оттисков путем переноса красителя при нагр. с печатной формы
на ткань, бумагу, строит. и иные материалы). На этом методе основано, в частности,
применение видеопринтеров для получения высококачеств. цветных копий на пленочных
носителях. Электрич. сигналы, поступающие в принтер с видеосистемы (напр., дисплея),
подводятся к термоголовке, точечные элементы к-рой нагревают нанесенный на рулонную
полимерную пленку слой красителей разл. цветов. Красители последовательно сублимируются
(в кол-ве, пропорциональном кол-ву энергии, подведенной к каждому элементу термоголовки)
и переносятся в газовой фазе к осн. носителю изображения. Метод обеспечивает
наиб. высокое среди всех принтеров качество изображения, позволяя воспроизводить
св. 16 млн. цветовых оттенков.
СД процессы протекают также
при газофазной полимеризации
, химических транспортных реакциях, химическом осаждении из газовой фазы
. При описании этих и иных процессов, сопровождающихся
хим. превращениями, в литературе иногда используют термины "хим. возгонка"
и "хим. десублимация".
Лит.: Гуйго Э.И.,
Журавская Н.К., Каухчешвили Э. И., Сублимационная сушка в пищевой промышленности,
2 изд., М., 1972; Евдокимов В. И., Химическая возгонка, М., 1984; Процессы сублимации
и десубли-мации в химической технологии. Обзорная информация, в. 9, М., 1985;
Горелик А. Г., Амитин А.В., Десублимация в химической промышленности, М., 1986;
Емяшев А. В., Газофазная металлургия тугоплавких соединений, М., 1987; Головашкин
А.И., "Ж. Всес. хим. об-ва им. Д.И.Менделеева", 1989, т. 34, № 4,
с. 481-92. А. Г. Горелик.
|

