СУКЦИНИМИД
(2,5-пирролидиндион,
имид янтарной к-ты), мол. м. 99,09; бесцв. кристаллы орторомбич. син-гонии (а = 0,75 нм, b = 0,962 нм, с = 1,275 нм, z - 8, пространств.
группа Pmmm); т.пл. 125 °С, т. кип. 287-288 °С, 157°С/10
мм рт.ст.; плота. 1,42 г/см3 (20°С); g 44,31 Н/м (126°С);
m 4,66·10-30 Кл·м (диоксан, 30 °С); ур-ние температурной
зависимости давления пара в интервале 416-561 К: lgp (мм рт. ст.) = 9,109-3491/T;
Сp 1,328 кДж/(кг·К) при 0-99,6 °С; 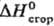 -1833 кДж/моль. С. хорошо
раств. в воде и этаноле, плохо-в диэтило-вом эфире, не раств. в СНС13.
С.-слабая к-та, К 2,38·10-10 (25 °С), с металлами образует
соли и комплексные соединения.
-1833 кДж/моль. С. хорошо
раств. в воде и этаноле, плохо-в диэтило-вом эфире, не раств. в СНС13.
С.-слабая к-та, К 2,38·10-10 (25 °С), с металлами образует
соли и комплексные соединения.
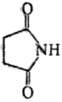
При восстановлении С.,
в зависимости от условий р-ции, образуются пирролидин, 2-пирролидон, пиррол
или g-ами-номасляная к-та:
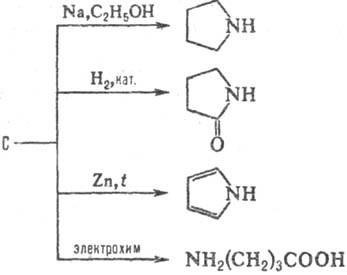
Галогенирование С. приводит
к N-галогенсукцинимидам (см. N-Галогенимиды
), взаимод. с Вr2
или NaBrO в щелочной среде при нагр.-к b-аланину NH2(CH2)2COOH
(см. Гофмана реакции
), действие щелочных солей алкилгалоге-нидов-к
N-алкилпроизводным.
При пропускании в расплав
С. Сl2 или Вr2 при 160°С образуются галогензамещенные
имиды малеиновой к-ты, взаимодействие С. с РСl5 дает 2,2,3,4,5-пентахлор-2H-пир-рол:
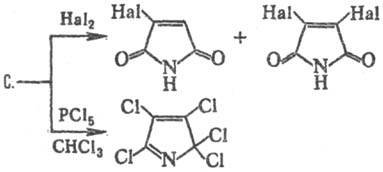
Обработка С. NH3
или СН3ОН приводит к размыканию цикла с образованием соотв. диамида
NH2CO(CH2)2CONH2 или метилового
эфира моноамида янтарной к-ты CH3OOC(CH2)2CONH2.
При действии на С. формальдегида образуется N-гидроксиметиленсукцинимид (в присут.
К2СО3) либо N,N-метилендисукцинимид (при 160°С).
Получают С. нагреванием
янтарной к-ты HOOC(CH2)2COOH или ее ангидрида в токе NH3
при 180-200 °С; сухой перегонкой диаммониевой соли или амида янтарной к-ты
либо мочевины; обработкой акрилонитрила водным р-ром NaCN; карбонилированием
акриламида в присут. Со.
Применяют С. гл. обр. для
получения N-хлор- и N-бромсукцинимидов, а также для синтеза гетероциклич. соединений
ряда пиррола. Нек-рые производные С., напр. N-сукцинил-3,5-дахлоранилин, используют
в качестве пестицидов.
См. также Имиды карболовых кислот
.
Лит.: Общая органическая
химия, пер. с англ., т. 4, М., 1983, с. 338-536. С. К. Смирнов.
|

