ТЕТРАГИДРОФУРФУРИЛОВЫЙ СПИРТ
(2-гидрокси-метилтетрагидрофуран, тетрагидрофуриловый спирт),
мол.м. 102,13; бесцв. жидкость; т.кип. 177-178°С, 80-82°С/20
мм рт. ст.; 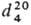 1,0535;
1,0535;
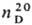 1,4517. Смешивается
с водой и большинством
орг. р-рителей.
1,4517. Смешивается
с водой и большинством
орг. р-рителей.
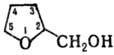
Для Т. с. наиб. характерны
расщепление цикла и р-ции по группе-ОН, напр.:
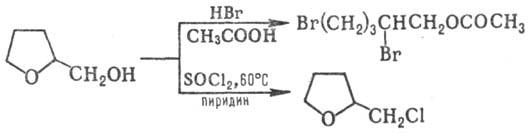
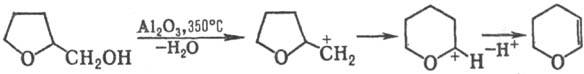
При нагр. (350-370 °С)
над А12О3 Т. с. претерпевает дегидратацию с послед. перегруппировкой
карбкатиона по Вагнеру -Меервейну и образованием 2,3-дигидропирана (выход 85-87%):
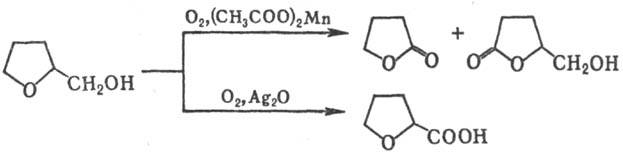
Осн. продукты жидкофазного
окисления Т.е. в присут. ацетата Мn или В2О3 при
120-140 °С-g-бутиролактон и g-гидроксиметил-g-бутиролактон;
в присут. Ag2O или Ag2O/Al2O3 с
выходом 60-80% образуется тетрагидрофу-ран-2-карбоновая к-та:
При пропускании смеси Т.е.
с NH3 над алюмохромовым катализатором при 400-450 °С с выходом
65-70% образуется смесь пиридина и пиперидина.
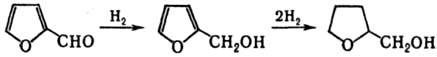
В пром-сти Т. с. получают
двустадийным гидрированием фурфурола в жидкой фазе (100-160 °С, 10-14 МПа)
в присут. скелетного Ni, модифицированного добавками Мо (10-15%), Сr (1-5%),
Си, Ti, W или металлов платиновой группы:
Т.с.-р-ритель для многих
орг. в-в, в т.ч. полимерных материалов, синтетич. каучуков, лаков, красителей
и др. Сложные эфиры Т. с.- пластификаторы для ПВХ.
Лит.: Успехи химии
фурана, под ред. Э. Я. Лукевица, Рига, 1978; Контактные реакции фурановых соединений,
под ред. М. В. Шиманской, Рига, 1985.
Р. А. Караханов, В.И.
Келарев.
|

