p -ЭЛЕКТРОННОЕ ПРИБЛИЖЕНИЕ
, квантовохим.
метод изучения энергетич. состояний ненасыщенных соед., в к-ром св-ва молекулы
соотносятся со строением системы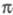 -орбита-лей.
В рамках молекулярных орбиталей методов
все орбитали молекулы, ядерная
конфигурация к-рой имеет плоскость симметрии, можно разделить на
-орбита-лей.
В рамках молекулярных орбиталей методов
все орбитали молекулы, ядерная
конфигурация к-рой имеет плоскость симметрии, можно разделить на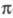 -орбитали,
меняющие знак при отражении в плоскости симметрии, и
-орбитали,
меняющие знак при отражении в плоскости симметрии, и -орбитали,
не меняющие знака. Для многих классов соед., напр. ненасыщенных углеводородов,
высшие занятые и низшие виртуальные (незанятые) орбитали относятся к
-орбитали,
не меняющие знака. Для многих классов соед., напр. ненасыщенных углеводородов,
высшие занятые и низшие виртуальные (незанятые) орбитали относятся к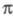 -типу,
а усредненное поле, создаваемое
-типу,
а усредненное поле, создаваемое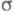 -электронами,
можно считать локально постоянным. Это позволяет пренебречь взаимным влиянием
-электронами,
можно считать локально постоянным. Это позволяет пренебречь взаимным влиянием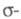 и
и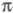 -электронных подсистем
при изучении низколежащих по энергии электронных состояний.
-электронных подсистем
при изучении низколежащих по энергии электронных состояний.
Для молекул, обладающих плоскостью симметрии,
выделение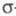 -
и
-
и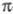 -орбиталей
не составляет трудностей. Напр., для плоской молекулы этилена
-орбиталей
не составляет трудностей. Напр., для плоской молекулы этилена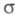 -орбитали
считаются построенными из гибридных sp2-орбиталей атома
С и 1s-орбиталей атомов Н, а
-орбитали
считаются построенными из гибридных sp2-орбиталей атома
С и 1s-орбиталей атомов Н, а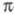 -орбитали
- из негибридизированных 2р-орби-талей атомов С. Для молекул, не имеющих
плоскости симметрии, строгое выделение системы
-орбитали
- из негибридизированных 2р-орби-талей атомов С. Для молекул, не имеющих
плоскости симметрии, строгое выделение системы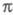 -орбиталей
невозможно. В этом случае для
-орбиталей
невозможно. В этом случае для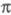 -Э.
п. используют такие орбитали, к-рые более всего напоминают р-орбитали
атомов. Напр., для пропилена
-Э.
п. используют такие орбитали, к-рые более всего напоминают р-орбитали
атомов. Напр., для пропилена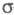 -орбитали
можно описать с помощью тех же орбиталей, что и в случае этилена, и sp3-орбиталей
атома С метильной группы. В качестве p-ороиталей
рассматривают негибридизированные 2p-орбитали атомов С.
-орбитали
можно описать с помощью тех же орбиталей, что и в случае этилена, и sp3-орбиталей
атома С метильной группы. В качестве p-ороиталей
рассматривают негибридизированные 2p-орбитали атомов С.
Мол. системы, для к-рых возможно разделение
орбиталей на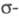 и
и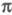 -орбитали,
наз. часто
-орбитали,
наз. часто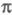 -электронными
системами или просто
-электронными
системами или просто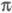 -системами.
Как правило,
-системами.
Как правило,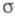 -орбитали
носят локализованный характер, обычно они двухцентровые.
-орбитали
носят локализованный характер, обычно они двухцентровые.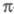 -Орбитали
существенно менее локализованы и могут иметь трех-, четырех- или многоцентровый
характер, что в химии связывают с понятием сопряжения связей
(бутадиен,
бензол и т. п.). При изменении строения молекулы (напр., введении заместителей)
изменения св-в связывают именно с
-Орбитали
существенно менее локализованы и могут иметь трех-, четырех- или многоцентровый
характер, что в химии связывают с понятием сопряжения связей
(бутадиен,
бензол и т. п.). При изменении строения молекулы (напр., введении заместителей)
изменения св-в связывают именно с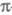 -орбиталями,
а изменением
-орбиталями,
а изменением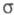 -орбиталей
пренебрегают. Взаимное влияние
-орбиталей
пренебрегают. Взаимное влияние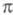 -орбиталей
и остальных мол. орбиталей учитывают как изменение св-в молекулы при введении
заместителя (поляризацию) или как дополнит. сопряжение, используя методы,
напр., возмущений теории
. Надежность результатов, получаемых в p-Э.
п., определяется тем, насколько удалены друг от друга локализованные мол.
орбитали, взаимодействующие с системой
-орбиталей
и остальных мол. орбиталей учитывают как изменение св-в молекулы при введении
заместителя (поляризацию) или как дополнит. сопряжение, используя методы,
напр., возмущений теории
. Надежность результатов, получаемых в p-Э.
п., определяется тем, насколько удалены друг от друга локализованные мол.
орбитали, взаимодействующие с системой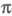 -орбиталей, а также тем, насколько различаются эти мол. орбитали по энергии.
-орбиталей, а также тем, насколько различаются эти мол. орбитали по энергии.
Как правило, в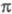 -Э.
п. для расчетов основного состояния молекулы используют полуэмпирические методы
квантовой химии, основанные на пренебрежении дифференциальным
перекрыванием атомных орбиталей. Расчет низколежащих возбужденных состояний
возможен с использованием конфигурационного взаимодействия метода
в
том его варианте, в к-ром однократно возбужденные электронные конфигурации
получают заменой занятых
-Э.
п. для расчетов основного состояния молекулы используют полуэмпирические методы
квантовой химии, основанные на пренебрежении дифференциальным
перекрыванием атомных орбиталей. Расчет низколежащих возбужденных состояний
возможен с использованием конфигурационного взаимодействия метода
в
том его варианте, в к-ром однократно возбужденные электронные конфигурации
получают заменой занятых -орбиталей
на аналогичные вакантные. К таким методам относится, напр., метод Паризе
ра-Парра-Попла (метод ППП). Взаимодействие
-орбиталей
на аналогичные вакантные. К таким методам относится, напр., метод Паризе
ра-Парра-Попла (метод ППП). Взаимодействие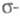 и
и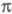 -орбиталей
проявляется как зависимость молекулярных интегралов
и геометрии
молекулы от
-орбиталей
проявляется как зависимость молекулярных интегралов
и геометрии
молекулы от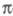 -электронной
плотности.
-электронной
плотности.
В связи с развитием расчетных методов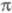 -Э.
п. вытесняется полуэмпирич. методами без выделения
-Э.
п. вытесняется полуэмпирич. методами без выделения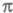 -системы
или неэмпирическими методами
. Однако для мол. систем большого размера
(полиацетилены, поликонденсиров. системы) учет всех взаимод. затруднен.
Для них обычно используют упрощенные варианты
-системы
или неэмпирическими методами
. Однако для мол. систем большого размера
(полиацетилены, поликонденсиров. системы) учет всех взаимод. затруднен.
Для них обычно используют упрощенные варианты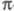 -Э.
п. Напр., в т. наз. приближении Хаббарда ненулевыми мол. интегралами считаются
лишь одноцентровые интегралы межэлектронного отталкивания. Еще более простым
является приближение Хюккеля, в к-ром двухэлектронными взаимод. вообще
пренебрегают, а в матрице эффективного гамильтониана, определяющего
-Э.
п. Напр., в т. наз. приближении Хаббарда ненулевыми мол. интегралами считаются
лишь одноцентровые интегралы межэлектронного отталкивания. Еще более простым
является приближение Хюккеля, в к-ром двухэлектронными взаимод. вообще
пренебрегают, а в матрице эффективного гамильтониана, определяющего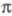 -орбиталь,
сохраняются лишь диагональные элементы и те из недиагональных, к-рые можно
соотнести с валентным штрихом в структурной ф-ле молекулы (см. Хюккеля метод
).
-орбиталь,
сохраняются лишь диагональные элементы и те из недиагональных, к-рые можно
соотнести с валентным штрихом в структурной ф-ле молекулы (см. Хюккеля метод
).
Упомянутые упрощенные варианты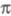 -Э.
п. предполагают определение полуэмпирич. параметров по результатам расчета
энергии
-Э.
п. предполагают определение полуэмпирич. параметров по результатам расчета
энергии -системы,
потенциалов ионизации или энергий возбуждения простых молекул (без заместителей).
-системы,
потенциалов ионизации или энергий возбуждения простых молекул (без заместителей).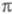 -Э.
п. служит для описания наиб. изменчивой, легко поляризуемой и относительно
независимой части электронного распределения молекулы. Корреляционные соотношения
позволяют соотнести энергию
-Э.
п. служит для описания наиб. изменчивой, легко поляризуемой и относительно
независимой части электронного распределения молекулы. Корреляционные соотношения
позволяют соотнести энергию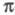 -системы
и распределение электронной плотности с хим. св-вами молекулы.
-системы
и распределение электронной плотности с хим. св-вами молекулы.
У многих мол. систем среди низших возбужденных
состояний есть такие, для описания к-рых необходим учет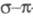 -возбуждений,
напр. если в
-возбуждений,
напр. если в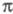 -систему
включается гетероатом с неподеленными парами электронов. В таких случаях
-систему
включается гетероатом с неподеленными парами электронов. В таких случаях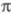 -Э.
п.
-Э.
п.
становится слишком грубым. То же можно
утверждать и для мол. систем с заметным переносом заряда при возбуждении.
У молекул, традиционно относимых к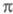 -системам,
высшие занятые
-системам,
высшие занятые -орбитали
могут лежать по энергии выше низших занятых
-орбитали
могут лежать по энергии выше низших занятых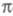 -орбиталей
(пример - бензол). При внеш. воздействии на такие молекулы необходим учет
изменения не только
-орбиталей
(пример - бензол). При внеш. воздействии на такие молекулы необходим учет
изменения не только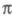 -орбиталей, но и
-орбиталей, но и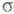 -орбиталей
(напр., при анализе магн. восприимчивости).
-орбиталей
(напр., при анализе магн. восприимчивости).
С 80-х гг. стали заметны две тенденции
в развитии методов изучения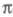 -электронных
систем. Первая - отказ от учета особой роли
-электронных
систем. Первая - отказ от учета особой роли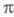 -орбиталей
и анализ молекулы как целого или же выделение группы низколежащих орбиталей
(или групп орбиталей) молекулы независимо от типа их симметрии. Вторая
тенденция - переход к чисто топологич. моделированию высших занятых и низших
виртуальных мол. орбиталей; топологич. моделирование связано с методами
типа метода Хюккеля и теориями реакционной способности, основанными на
корреляционных соотношениях или принципах сохранения орбитальной симметрии
(см. Вудворда-Хофмана правила
).
-орбиталей
и анализ молекулы как целого или же выделение группы низколежащих орбиталей
(или групп орбиталей) молекулы независимо от типа их симметрии. Вторая
тенденция - переход к чисто топологич. моделированию высших занятых и низших
виртуальных мол. орбиталей; топологич. моделирование связано с методами
типа метода Хюккеля и теориями реакционной способности, основанными на
корреляционных соотношениях или принципах сохранения орбитальной симметрии
(см. Вудворда-Хофмана правила
).
Лит.: Дьюар М., Теория молекулярных
орбиталей в органической химии, пер. с англ., М., 1972; Полуэмпирические
методы расчета электронной структуры, пер. с англ., т. 1-2, М., 1980; Травень
В. Ф., Электронная структура и свойства органических молекул, М., 1989.
В. И. Пупышев.
|

