ТРОПОЛОНЫ
(2-гидрокситропоны),
семичленные сопря-женные циклич. гидроксикетоны; относятся к небензоидным ароматич.
соединениям.
Простейший T. - 2-гидроксициклогепта-2,4,6-триен-1-он
(ф-ла I), бесцв. иглы; т. пл. 50-51 0C; легко возгоняется;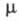 12,37·10-30
Кл·м; раств. в воде и орг. р-рителях; рKa 6,92.
12,37·10-30
Кл·м; раств. в воде и орг. р-рителях; рKa 6,92.
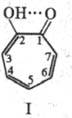
Ядро трополона - правильный
семиугольник, длины связей (нм) 0,14 (С —С), 0,125 (C = O), 0,134 (С —О), что
свидетельствует об асимметричности молекулы.
Трополоновое кольцо
присутствует в нек-рых природных соед., напр, в колхицине, выделенном из безвременника
осеннего Colchicum Autumnale; в древесине кедра содержатся терпеновые T. (3-,
4- и 5-изопропилтропо-лоны, туяплицины); метаболитами разл. видов плесени явля-ются
2,6-дигидрокситропон-4-карбоновая (стипитатовая) к-та и 2,6,7-тригидрокситропон-З-карбоновая
(пуберуловая) к-та. Хим. св-ва T. определяются наличием системы сопряжен-ных
связей и внутримол. водородной связи. T. протонируются сильными к-тами; с основаниями,
подобно фенолам, образу-ют анионы:
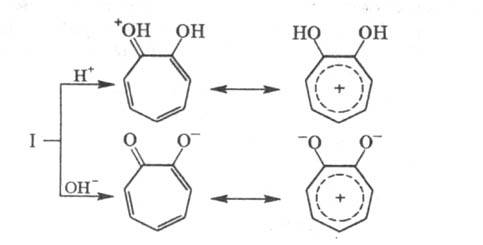
С конц. HCl и пикриновой
к-той T. дают оксониевые соли, с солями металлов со степенями окисления 2 и
3 - комплек-сные соед.; медный комплекс используют для выделения T.
Восстановление T. протекает
с трудом; окисление в жест-ких условиях (KMnO4, CrO3)
приводит к расщеплению коль-ца, что используют для установления строения природных
T.
T. проявляют ароматич.
характер, т.е. при формальной ненасыщенности часто не обнаруживают ее в своих
р-циях. Подобно фенолам, вступают в r-ции электроф. замещения: галогенирование,
нитрование, нитрозирование, амино- и гид-роксиметилирование, р-ция Раймера -
Тимана, не дают обыч-ных р-ций на карбонильную группу (не образуют гидразонов
и семикарбазонов), трудно гидрируются. Вследствие электро-нодефицитности кольца
T. не удается провести р-ции Фри-деля - Крафтса и Гаттермана, перегруппировку
Фриса. T. не сульфируются H2SO4 и SO3 (сульфируются
сульфаминовой к-той). В то же время T. проявляют нек-рые св-ва ненасыщ. соединений,
напр, вступают в диеновый синтез.
Получают трополон из пробковой
к-ты по схеме:
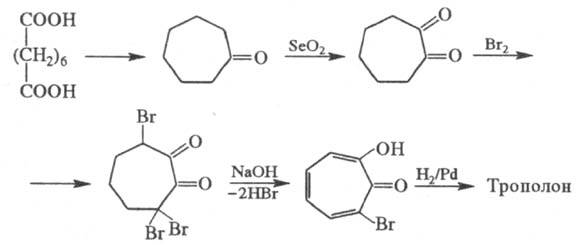
T. образуется также окислением
тропилидена (циклогеп-татриена) KMnO4; взаимод. 1,2-диметоксибензола
с диазоуксусным эфиром, образующееся производное циклогептатрие-на бромируют,
омыляют и декарбоксилируют; циклизацией диэтилового эфира пимелиновой к-ты с
послед, бромирова-нием и каталитич. дебромированием.
T. обладают антимитотич.
(препятствуют делению клеток), бактериостатич. и фунгицидным действием.
Лит.: По сон П.,
Химия тропонов и трополонов, пер. с англ., M., 1956; Небензоидные ароматические
соединения, пер. с англ., M., 1963.
И. С. Ахрем.
|

