ВОССТАНОВИТЕЛИ
, в-ва, отдающие электроны в окислит.-восстановит.
р-циях. Относит. восстановит. способность двух и более в-в определяется
путем сравнения изменений энергии Гиббса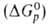 при р-циях этих в-в с одним и тем же окислителем, а в случае р-ций с участием
простых в-в - энергией Гиббса образования
при р-циях этих в-в с одним и тем же окислителем, а в случае р-ций с участием
простых в-в - энергией Гиббса образования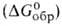 продуктов окисления простого в-ва (оксидов, галогенидов и т.п.). Чем больше
продуктов окисления простого в-ва (оксидов, галогенидов и т.п.). Чем больше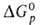 или абс. величина
или абс. величина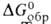 ,
тем более активным В. является данное в-во. так, при обычных условиях в
р-циях nМ + mМFn -> nMFm + mMкальций
- более активный В. фторидов металлов (
,
тем более активным В. является данное в-во. так, при обычных условиях в
р-циях nМ + mМFn -> nMFm + mMкальций
- более активный В. фторидов металлов ( CaF2, отнесенная к одному атому фтора, - 584,2 кДж/моль), чем
Mg (-535,5 кДж/моль) и А1 (-477,1 кДж/моль), но менее активный, чем Li
(для LiF
CaF2, отнесенная к одному атому фтора, - 584,2 кДж/моль), чем
Mg (-535,5 кДж/моль) и А1 (-477,1 кДж/моль), но менее активный, чем Li
(для LiF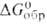 — 588,0 кДж/моль). В случае электрохим. р-ций для сравнения восстановит.
способности в-в используют стандартный электродный потенциал Е°. Чем
больше абс. величина E° полуреакции восстановления с участием данного в-ва,
тем более сильными восстановит, св-вами это в-во обладает.
— 588,0 кДж/моль). В случае электрохим. р-ций для сравнения восстановит.
способности в-в используют стандартный электродный потенциал Е°. Чем
больше абс. величина E° полуреакции восстановления с участием данного в-ва,
тем более сильными восстановит, св-вами это в-во обладает.
К сильным В. принадлежат щелочные и щел.-зем. металлы, Al, Si, С, Н2
и ряд др. простых в-в, гидриды металлов и соед., содержащие неметаллы с
отрицат. степенями окисления ( и др.). Очень сильной восстановит. способностью обладают р-ры, содержащие
своб. или сольватированные электроны, напр. аммиачные р-ры щелочных и щел.-зем.
металлов (см. Аммиак
), а также атомарный водород.
и др.). Очень сильной восстановит. способностью обладают р-ры, содержащие
своб. или сольватированные электроны, напр. аммиачные р-ры щелочных и щел.-зем.
металлов (см. Аммиак
), а также атомарный водород.
Существуют в-ва, к-рые в одной и той же окислит.-восстановит. р-ции
являются одновременно и В., и окислителями. В молекуле таких в-в содержатся
атомы, отдающие и присоединяющие электроны, напр.:
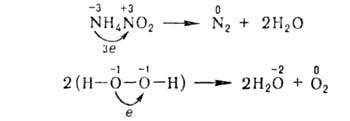
В разл. процессах одни и те же в-ва могут быть В. или окислителями,
напр. вода в р-циях: Н2O(В.) + F2 -> 2HF + 1/2O2
4Н2О(окислитель)
+ 3Fe -> Fe3O4 + Н2
В. применяют: для восстановления Fe из руд (С, Н2, водяной
и прир. газы, СО, пропан, бутан); при получении цветных и редких металлов
в процессах металлотермии
(С, Si, Al, Na, Ca, Mg, La); при выделении
(цементации) цветных металлов из водных р-ров их солей (Fe, Zn); при получении
металлов, их низших оксидов и галогенидов и при хим. осаждении металлов,
нитридов и карбидов из газовой фазы (Н2, NH3, CH4
и др.); при проведении разл. хим. процессов в р-рах (SnCl2,
FeSO4, H2SO3, N2H4,
NH2OH, HCOOH, H2S и др.); в орг. синтезе (Н2,
Na, Zn, Li[AlH4], Na[BH4], B2H6
и др.); как проявляющие в-ва в фотографии (гидрохинон, амидол, метол, фенидон
и др.). В хим. источниках тока В. (Li, Na, Zn, нек-рые др. металлы, а также
сплавы) входят в состав анодов.
Лит.: То у б М. Л., Механизмы неорганических реакций, пер. с
англ., М., 1975, с. 181-82. Э. Г. Раков, Б. Д. Степин.
|

