АНТРАХИНОНКАРБОНОВЫЕ КИСЛОТЫ
. Практич. значение имеют
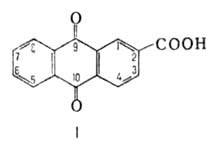
антрахинон-2-карбоновая к-та (2-А.; ф-ла I), ее замещенные-1-аминоантрахинон-2-
и 1-амино-4-бромантрахинон-2-карбоновые к-ты, а также используемая в лаб.
практике антрахинон-1-карбоновая к-та (1-А.). 1-А. и 2-А.-светло-желтые
кристаллы (см. табл.); плохо раств. в воде, раств. в уксусной кислоте,
ДМФА, конц. H2SO4; их Na-соли умеренно раств. в воде.
А. к. с РОС13, РС15 образуют хлорангидриды, к-рые
при действии спиртов или аминов превращ. соотв. в эфиры или амиды. 1-А.
и 2-А. восстанавливаются Zn в водном р-ре NH3 до антраценкарбоновых
к-т, действием Na2S2O4
в р-ре NaOH - до
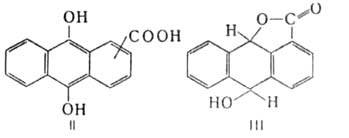
9,10-антрагидрохинонкарбоновых к-т (П). 1-А. под действием Sn в конц. НС1
восстанавливается до антрон-4-карбоновой к-ты и лактона 9,10-дигидро-9-антрол-1-карбоновой
к-ты (III). Нитрование 1-А. в конц. H2SO4 при 95°С
дает в осн. 5-нитроантрахинон-1-карбоновую к-ту. Сульфирование 2-А. 40%-ным
олеумом при 100°С приводит к смеси 2-карбоксиантрахинон-6- и 1-А. способна
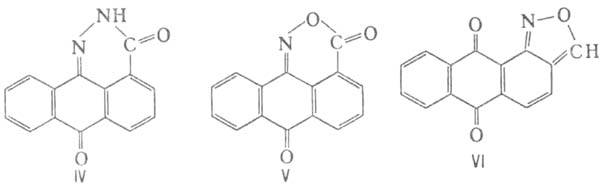
к образованию гетероциклич. соединений антрона, напр. с гидразингидратом-пиридазонантрона
(IV), с гидроксиламином - оксазонантрона (V). 2-А. при2-карбоксиантрахинон-7-сульфокислот.
нагр. с NaOH до 280-300°С декарбоксилируется до антрахинона. В 1-амино-4-бромантрахинон-2-карбоновой
к-те при взаимод. с аминами в присут. соединений Сu атом брома замещается
на остаток амина и образуются продукты, используемые как кислотные красители.
Хлорангидрид 1-аминоантрахинон-2-карбоновой к-ты конденсируется по р-ции
Фриделя - Крафтса с бензолом, образуя 1-амино-2-бензоилантрахинон-промежут.
продукт в синтезе дисперсных красителей. Хлорангидрид 2-А. применяют в
произ-ве кубовых красителей.
СВОЙСТВА АНТРАХИНОНКАРБОНОВЫХ КИСЛОТ
|
Заместители и их положение в ядре антрахинона
|
Мол. м.
|
Т.пл., °С
|
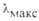
, нм |
|
1-СООН
|
252,21
|
294
|
329
|
|
2-СООН
|
252,21
|
292
|
324
|
|
1-NН2, 2-СООН
|
267,23
|
286
|
486
|
|
I-NH2, 2-СООН, 4-Вг
|
346,14
|
325
|
506
|
Получают 1-А. окислением бензантрона в разб. H2SO4 при
70°С действием СrО3; окислением 1-метилантрахинона разб. HNO3
при 160°С под давлением; диазотированием 1-аминоантрахинона с послед. заменой
диазогруппы на CN-группу и омылением ее в р-ре H2SO4;
циклизацией 3-бензоилфталевой или 2-бензоилизофталевой к-ты. 2-А. синтезируют
окислением 2-метилантрахинона действием СгО3 в СН3СООН
или циклизацией бензофенон-2,4-дикарбоновой к-ты в 5%-ном олеуме при 110-120°С
1-Аминоантрахинон-2-карбоновую к-ту получают внутримолекулярным превращ.
1-нитро-2-метилантрахинона в 60%-ном олеуме с образованием антра[1,2-с]изоксазол-6,11-диона
(VI) с послед. его щелочным гидролизом. Бромированием 1-аминоантрахинон-2-карбоновой
к-ты в конц. H2SO4 при 90°С синтезируют 1-амино-4-бромантрахинон-2-карбоновую
к-ту.
Лит.: Горелик М. В., Химия антрахинонов и их производных, М.,
1983. С. И. Попов.




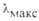 , нм
, нм
