АСПАРАГИН
(от греч. asparagos - спаржа) (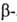 амид
аспара-гиновой к-ты, Asn, N) H2NOCCH2CH(NH2)COOH,
мол. м. 132,12; бесцв. кристаллы. Для D, L-, L- и D-A. т.пл. соотв. 220°С
(моногидратХ 233 °С (с разл.) и 215°С; для L- и D-A.
амид
аспара-гиновой к-ты, Asn, N) H2NOCCH2CH(NH2)COOH,
мол. м. 132,12; бесцв. кристаллы. Для D, L-, L- и D-A. т.пл. соотв. 220°С
(моногидратХ 233 °С (с разл.) и 215°С; для L- и D-A.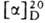 соотв. 4-3 Г (концентрация 10 г в 100 мл Зн. НС1) и + 5,41° (концентрация
1,3 г в 100 мл Н2О). А. раств. в воде, к-тах, не раств. в орг.
р-рителях; при 26 °С рКа 2,02 (СООН), 3, 8 (NH2);
p/ 5,41.
соотв. 4-3 Г (концентрация 10 г в 100 мл Зн. НС1) и + 5,41° (концентрация
1,3 г в 100 мл Н2О). А. раств. в воде, к-тах, не раств. в орг.
р-рителях; при 26 °С рКа 2,02 (СООН), 3, 8 (NH2);
p/ 5,41.
А. - типичная алифатич.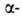 аминокислота.
Образует окрашенные продукты в биуретовой р-ции. При нагр. солей А. с к-тами
или щелочами гидролизуется амидная связь и выделяется NH3, что
используется для количеств. определения А. При синтезе из А. пептидов наряду
с
аминокислота.
Образует окрашенные продукты в биуретовой р-ции. При нагр. солей А. с к-тами
или щелочами гидролизуется амидная связь и выделяется NH3, что
используется для количеств. определения А. При синтезе из А. пептидов наряду
с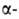 NH2 -
группой защищают
NH2 -
группой защищают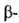 амидную
группу, для чего в нее вводят бензгидрильную, 4,4-диметоксибензгидрильную
или ксантенильную группу.
амидную
группу, для чего в нее вводят бензгидрильную, 4,4-диметоксибензгидрильную
или ксантенильную группу.
L-А.-кодируемая аминокислота, встречается во всех организмах в своб.
виде (в проростках вики - до 28%) и в составе белков.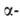 Амид
аспарагиновой к-ты (изоаспарагин, iAsn) и D-A. входят в состав гликопептидов
клеточных стенок нек-рых бактерий. L-A. в организме животных связывает
NH3 и переносит его к почкам. Биосинтез осуществляется в результате
амидирования аспарагиновой к-ты.
Амид
аспарагиновой к-ты (изоаспарагин, iAsn) и D-A. входят в состав гликопептидов
клеточных стенок нек-рых бактерий. L-A. в организме животных связывает
NH3 и переносит его к почкам. Биосинтез осуществляется в результате
амидирования аспарагиновой к-ты.
L-A. может быть выделен в виде нерастворимой Сu-соли из белковых гидролизатов.
D, L-A. получают из щавелевоуксусной к-ты. В спектре ЯМР L-A. в D2O
хим. сдвиги протонов у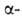 атома
углерода составляют 3,579 м.д., у
атома
углерода составляют 3,579 м.д., у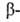 атома - 2,663 и 2,436 м.д. L-A. применяют для синтеза пептидов, в смеси
с др. аминокислотами - для парэнтерального питания. Впервые выделен из
белка эдестина М. Дамодара-ном в 1932. Мировое произ-во L-A. ок. 50 т/год
(1982). В. В. Баев.
атома - 2,663 и 2,436 м.д. L-A. применяют для синтеза пептидов, в смеси
с др. аминокислотами - для парэнтерального питания. Впервые выделен из
белка эдестина М. Дамодара-ном в 1932. Мировое произ-во L-A. ок. 50 т/год
(1982). В. В. Баев.
|

