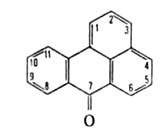
БЕНЗАНТРОН
(бензо[de]антрацен-7-он, мезобензантрон), мол. м.
230,20; желтые кристаллы; т. пл. 170-171 °С (с возгонкой);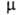 11,62*10-30 Кл*м (бензол; 25°С); раств. в спирте, хлорбензоле,
уксусной к-те, не раств. в воде. В УФ-спектре
11,62*10-30 Кл*м (бензол; 25°С); раств. в спирте, хлорбензоле,
уксусной к-те, не раств. в воде. В УФ-спектре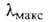 при
230 нм (lg
при
230 нм (lg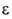 4,52),
253 нм (lg
4,52),
253 нм (lg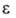 4,30), 282 нм (lg
4,30), 282 нм (lg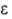 3,90), 306 нм (lg
3,90), 306 нм (lg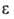 3,90), 395 нм (lg
3,90), 395 нм (lg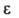 4,01).
Б.-слабое основание; в конц. H2SO4 присоединяет протон
с образованием р-ра с красной флуоресценцией, что используется для качеств.
определения Б. В апротонных р-рителях образует окрашенные комплексы с С13ССООН,
IC1, с хлоридами Fe(III), Sn(IV), Zn(II) и др.; связь в комплексах осуществляется
по кислороду карбонильной группы. Окисляется хромовой к-той в среде СН3СООН
или разб. H2SO4 до антрахинон-1-карбоновой к-ты,
восстанавливается щелочным раствором Na2S2O4
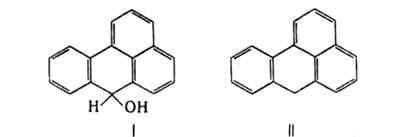
до дигидробензантрона (ф-ла I), Zn-пылью - до бензантрена (II).
4,01).
Б.-слабое основание; в конц. H2SO4 присоединяет протон
с образованием р-ра с красной флуоресценцией, что используется для качеств.
определения Б. В апротонных р-рителях образует окрашенные комплексы с С13ССООН,
IC1, с хлоридами Fe(III), Sn(IV), Zn(II) и др.; связь в комплексах осуществляется
по кислороду карбонильной группы. Окисляется хромовой к-той в среде СН3СООН
или разб. H2SO4 до антрахинон-1-карбоновой к-ты,
восстанавливается щелочным раствором Na2S2O4
до дигидробензантрона (ф-ла I), Zn-пылью - до бензантрена (II).
Электроф. реагенты замещают атомы Н в положениях 3 и 9. Так, бромированием
суспензии Б. в смеси СН3СООН и НС1 при 70°С получают 3-бромбензантрон
(т. пл. 173°С; выход 96%), а в конц. H2SO4 или в
хлорсульфоновой к-те при 0-40°С (кат.-I2)-3,9-дибромбензантрон
(т. пл. 255-256°С; выход 98%). Атомы брома в этих соединениях очень подвижны,
что используют в произ-ве кубовых красителей. Б. сульфируется конц. H2SO4
до бензантрон-9-сульфокислоты, хлорсульфоновой к-той в среде о-дихлорбензола
- до бензантрон-3-сульфокислоты, олеумом-до бензантрон-3,9-дисульфокислоты,
нитруется 87%-ной HNO3 в нитробензоле при 40-50°С до 3-нитропроизводного.
Нуклеоф. реагенты замещают атом Н в положениях 2 и 4. Так, при прямом аминировании
образуется 4-аминобензантрон, при взаимод. с анилином-4-фениламинобензантрон.
При сплавлении со щелочью в присут. безводного CH3COONa при
225°С Б. конденсируется до виолантрона - важного красителя для хлопка (см. Полициклические кубовые красители
). В присут. КОН реагирует с соединениями,
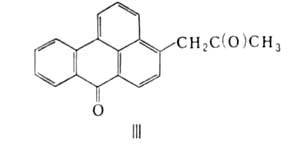
имеющими подвижный атом Н, напр. с ацетоном получают кетон ф-лы III. У
Б. слабо выражены св-ва, характерные для кетонов, т.е. он не реагирует
с NaHSO3, а оксим образует с трудом (выход 30%) при кипячении
в пиридине с гидроксиламином в течение 20 ч.
В пром-сти Б. получают конденсацией антрахинона с глицерином в конц.
H2SO4 при 110-115°С в присут. восстановителя (CuSO4
+ Zn); выход 89%. Лаб. синтез: постепенное нагревание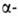 бензоилнафталина
(кат. - А1С13) до 150°С; выход 76%. Б. - исходное соединение
в производстве важных кубовых красителей (т. наз. группы бензантрона).
Для Б. ниж. КПВ 20 г/м3. Вызывает дерматиты, экземы; ЛД50
603 мг/кг (белые мыши, внутрибрюшинно); ПДК в водоемах 0,05 мг/л.
бензоилнафталина
(кат. - А1С13) до 150°С; выход 76%. Б. - исходное соединение
в производстве важных кубовых красителей (т. наз. группы бензантрона).
Для Б. ниж. КПВ 20 г/м3. Вызывает дерматиты, экземы; ЛД50
603 мг/кг (белые мыши, внутрибрюшинно); ПДК в водоемах 0,05 мг/л.
Лит.: КларЭ., Полициклические углеводороды, т. 2, М., 1971, с.
373; Kirk-Othmer encyclopedia, 3 ed, v. 2, N.Y., 1978, p. 742. H.H.
Артамонова.
|

