БЛАГОРОДНЫЕ ГАЗЫ
(инертные газы, редкие газы), хим. элементы
VIII гр. периодич. системы: гелий
(Не), неон
(Ne), аргон
(Аr),
криптон
(Кr), ксенон
(Хе), радон
(Rn). В природе образуются
в результате разл. ядерных процессов. Воздух содержит 5,24*10-4%
по объему Не, 1,82*10-3% Ne, 0,934% Аr, 1,14-10-4%
Кг, 8,6*10-6% Хе, 6*10-20% Rn. Космос более богат
Б. г., чем атмосфера Земли. Б. г. содержатся также в прир. газах и нек-рых
минералах.
Атомы Б. г. имеют полностью заполненные внеш. электронные оболочки (s2
для Не и s2p6 для всех остальных), что обусловливает
их низкую реакционную способность. Б.г. - одноатомные газы без цвета и
запаха (нек-рые их характеристики приведены в таблице; см. также статьи об отдельных представителях). Они относительно трудно сжижаются, но тем
легче, чем больше их атомная масса. Кристаллизуются в кубич. гранецентрированной
решетке; пространств, группа Рт3т. Значения Сp° не зависят
от т-ры до 6000 К и выше. Б. г. адсорбируются на активном угле и цеолитах
при низких т-рах; энтальпия адсорбции на угле (кДж/моль): Ne 4,72 (91 К),
Аr 16,43 (168 К), Кr 22,24 (223 К), Хе 36,53 (248 К), Не 2,26 (ниже 50
К). Это св-во используется для разделения Б. г. и их очистки. Б. г.-хорошие
диэлектрики (р 1018*1020 Ом*см). Они диамагнитны.
Степень сжимаемости для Не и Ne больше 1, для Аr, Кr, Хе - меньше 1 (273
К; 0,1-30 МПа). Относительно хорошо раств. в воде (р-римость быстро возрастает
от Не к Rn), лучше-во многих орг. р-рителях (бензин, толуол, спирт, бензол
и др.). Жидкий Не - единств. в-во, затвердевающее только под давлением
выше 2,5 МПа. Он обладает уникальным свойством - образует квантовую жидкость,
т.е. жидкость, в которой в макроскопическом объеме проявляются квантовые
свойства составляющих ее атомов.
Б. г. (кроме Не) образуют неустойчивые соед. включения (клатраты) с
водой и орг. р-рителями. Степень заполнения атомами Б. г. полостей кристаллич.
решеток соответствующих соединений определяет состав образующегося клатрата,
напр. Аr*4У, Кr*5,6У, Хе*3У (У = С6Н5ОН). Получены
гидраты типа Х*5,75Н2О, У*2Х*17Н2О, где Х - атом
Б.г. (кроме Не), У-СН3СОСН3, СНС13, СН3СООН,
СС14 и др. С фенолом и гидрохиноном выше 313 К образуются клатраты,
близкие по составу к Х*3У [X = Аr, Кr, Хе; У = = С6Н4(ОН)2].
Разработан метод получения клатратов при невысоких давлениях газа - изоморфное
соосаждение Б. г. с его аналогами в кристаллохим. отношении - H2S,
НВr, СО2, НС1, SO2, CH4. Таким путем получены
Х*6Н2О (X = Ne, Ar, Rn), X*2С6Н5СН3
(X = Хе, Rn), Rn -3C1C6H4OH и др. Различная способность
Б. г. к образованию клатратов м.б. использована для их разделения и выделения
из смесей.
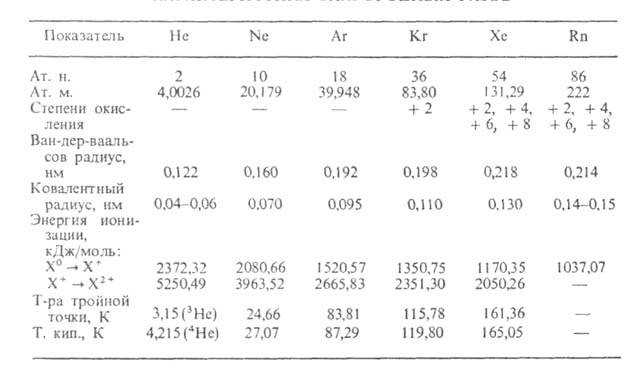
ХАРАКТЕРИСТИКА БЛАГОРОДНЫХ ГАЗОВ
К соед. включения относятся также т. наз. криптонаты, образующиеся при
бомбардировке ряда твердых в-в (металлов, стекол, каучуков, пластиков,
белков и др.) ионизованными атомами Б. г. при высоких т-pax и давлениях;
атомы Б. г. диффундируют в твердое в-во на глубину 102-103
нм.
Способность Б. г. к образованию хим. соед. понижается от Хе к Аг (самым
активным должен быть Rn, однако из-за высокой радиоактивности его св-ва
изучены мало; известны лишь фториды). наиб. число соед. получено для Хе
(фториды, хлориды, оксиды, оксофториды, фосфаты, перхлораты, фторсульфонаты,
ксенаты, перксенаты и др.) В присут. катализаторов (к-т Льюиса) Хе энергично
взаимод. уже при нормальных условиях с F2. Криптон реагирует
только с элементарным фтором при низких т-рах. Различная реакционная способность
Б. г. по отношению к F2 и нек-рым фторсодержащим окислителям
м. б. использована для их разделения, утилизации радиоактивных изотопов
и очистки. Напр., Хе с SbO2F6 взаимод. с образованием
твердого нелетучего соед. XeF2*2SbF5, а Кr такого
в-ва не образует. Аналогичную р-цию с Rn предложено использовать для очистки
атмосферы урановых рудников. Газы Rn и Хе окисляются также с помощью К2
[NiF6], Cs2 [CoF6], К3 [CuF6]
и др. Для улавливания радиоактивных изотопов благородных газов, в основном
133Хе
и 85Кr - продуктов деления U в ядерных реакторах, наряду с наиб.
эффективными методами криогенной дистилляции и адсорбции на активном угле
перспективны также избирательное поглощение хладонами, диффузионные методы,
образование клатратов и других химических соединений.
Б. г. образуют эксимеры под действием пучка электронов, УФ-излучения
или электрич. разряда на их смеси с галогенами, О2, фторсодержащими
соед. Молекулы эксимеров существуют только в электронно-возбужденном состоянии.
Переход из возбужденного состояния в несвязанное сопровождается когерентным
излучением в широкой области спектра (100-600 нм), что используется для
генерации лазерного излучения. Лазерное действие получено для KrF* (248
нм), Kr2F* (420 нм), ХеС1* (308 нм), KrCl* (222 нм) и др.
Б. г. (кроме Не) получают как побочные продукты при произ-ве N2
и О2 из воздуха. Гелий выделяют из подземных гелионосных газов.
Используют Б. г. в кач-ве инертной среды в металлургии, атомной и ракетной
технике, в произ-ве полупроводниковых материалов и др., как наполнитель
в электронике, электротехнике и др., рабочее в-во в лазерной технике.
При повышенных давлениях Б. т. оказывают вредное действие на нервную
систему (усиливающееся с увеличением атомной массы элемента), к-рое быстро
проходит при вдыхании чистого воздуха.
Лит.: Фастовский В. Г., Ровинский А. Е., Петровски и Ю. В., Инертные
газы, 2 изд., М., 1972; Нейдинг А. Б., Соколов В. Б., "Успехи химии", 1974,
т. 43, № 12, с. 2146-94; Легасов В. А., "Вестник АН СССР", 1976, в. 12,
с. 3-16; Елецкий А. В., "Успехи физических наук", 1978, т. 125, в. 2, с.
279-314; Смирнов Б. М., "Успехи физических наук", 1983, т. 139, а 1, с.
53-81; Bartlett N., Sladky F. О., The chemistry of krypton, xenon and radon,
в кн.: Comprehensive inorganic chemistry, v. 1, Oxf.-[a.o.], 1973. В.Б.
Соколов.

